
A、CS2的比例模型: |
| B、乙醇的结构简式:C2H6O |
| C、核内有8个中子的碳原子:86C |
| D、HClO的结构简式:H-Cl-O |
 ,故A正确;
,故A正确;

科目:高中化学 来源: 题型:
 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )| A、稀释前,c(HX)=0.01 mol/L |
| B、稀释10倍,HX溶液的pH=3 |
| C、a、b两点:c(X-)>c(Cl-) |
| D、溶液的导电性:a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA | ||
| B、常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA | ||
| C、标准状况下,2.24L的CCl4中含有的C-Cl键数为0.4NA | ||
D、将CO2通过Na2O2使其增重a克时,反应中转移电子数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性KMnO4溶液与H2O2反应:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O |
| B、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| C、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| D、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
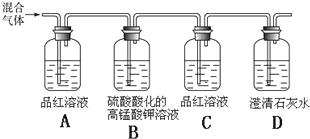
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、AlO2- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- |
| D、中性透明溶液:K+、HCO3-、NO3-、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com