
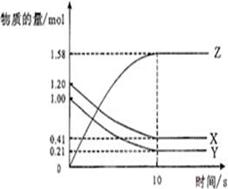
如右图所示,某温度下,物质的量分别是
1.2mol的气体X和物质的量为1.0mol的气体Y,
在2L密闭容器中反应生成气体Z,反应5min
后测得n(X) =0.4mol,n(Y)=0.2mol,生成的
n(Z)=1.6mol,则该反应的反应物为
该反应的化学方程式可表示为
,反应在10分钟内的化学反应速率用Z来表示则V(Z)= 。
科目:高中化学 来源:2012-2013学年浙江省桐乡一中高一下学期期中考试化学文科试卷(带解析) 题型:填空题
如右图所示,某温度下,物质的量分别是1.2mol的气体X和物质的量为1.0mol的气体Y,在2L密闭容器中反应生成气体Z,反应5min后测得n(X) =0.4mol,n(Y)=0.2mol,生成的n(Z)=1.6mol,则该反应的化学方程式可表示为 ,反应在10分钟内的化学反应速率用Z来表示则V(Z)= 。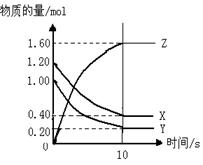
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高一下学期期中考试化学文科试卷(解析版) 题型:填空题
如右图所示,某温度下,物质的量分别是1.2mol的气体X和物质的量为1.0mol的气体Y,在2L密闭容器中反应生成气体Z,反应5min后测得n(X)
=0.4mol,n(Y)=0.2mol,生成的n(Z)=1.6mol,则该反应的化学方程式可表示为 ,反应在10分钟内的化学反应速率用Z来表示则V(Z)= 。
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(1)0.1mol/L Na2CO3溶液呈 (填“酸性”、“碱性”或“中性”),其原因是 (用离子方程式表示)
(2)氢氧燃料电池是利用氢能的一种重要方式。请写出氢氧燃料电池(电解质溶液为KOH溶液)的负极的电极反应式 。
(3)某温度下的水溶液中,c(H+)=10-xmol/L,
c(OH-)=10-y mol/L。x与y的关系如右图所示:

该温度下水的离子积为 ;该温度下0.01 mol/L NaOH溶液的pH为 。
(4)如右图装置,已知两电极上发生的电极反应分别为:a极:Cu2++2e-= Cu
b极:Fe-2e-= Fe2+
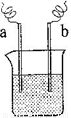
该装置中原电解质溶液一定含有 (填序号)
A. Cu2+ B.Na+ C.Fe2+ D. Ag+
(5)硫酸钡在水中存在沉淀溶解平衡:BaSO4(s)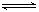 Ba 2+ (aq)+ SO42-(aq) 25℃
时,BaSO4的Ksp=1.1×l0—10,在0.1 mol·L一1硫酸溶液中,钡离子的浓度最大可达到
mol·L一1
Ba 2+ (aq)+ SO42-(aq) 25℃
时,BaSO4的Ksp=1.1×l0—10,在0.1 mol·L一1硫酸溶液中,钡离子的浓度最大可达到
mol·L一1
查看答案和解析>>
科目:高中化学 来源:2010年江西上高二中、新余钢铁中学高三年级全真模拟(理综)化学部分 题型:填空题
(1)0.1mol/L Na2CO3溶液呈 (填“酸性”、“碱性”或“中性”),其原因是 (用离子方程式表示)
(2)氢氧燃料电池是利用氢能的一种重要方式。请写出氢氧燃料电池(电解质溶液为KOH溶液)的负极的电极反应式 。
(3)某温度下的水溶液中,c(H+)=10-xmol/L,
c(OH-)=10-y mol/L。x与y的关系如右图所示:

该温度下水的离子积为 ;该温度下0.01 mol/L NaOH溶液的pH为 。
(4)如右图装置,已知两电极上发生的电极反应分别为:a极:Cu2++2e-= Cu
b极:Fe-2e-= Fe2+

该装置中原电解质溶液一定含有 (填序号)
A. Cu2+ B.Na+ C.Fe2+ D. Ag+
(5)硫酸钡在水中存在沉淀溶解平衡:BaSO4(s) Ba 2+ (aq)+ SO42-(aq) 25℃
时,BaSO4的Ksp=1.1×l0—10,在0.1 mol·L一1硫酸溶液中,钡离子的浓度最大可达到
mol·L一1
Ba 2+ (aq)+ SO42-(aq) 25℃
时,BaSO4的Ksp=1.1×l0—10,在0.1 mol·L一1硫酸溶液中,钡离子的浓度最大可达到
mol·L一1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com