
A. C和 C和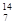 N的质量数相同,中子数不同 N的质量数相同,中子数不同 |
| B.IA族元素的金属性一定比IIA族元素的金属性强 |
| C.同周期主族元素的原子形成的简单离子电子层结构相同 |
| D.HCl、H2S、PH3的热稳定性由弱到强 |
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | Q | R | |
| T | | | W |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.075 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +5、+3 | +6、-2 | -2 |
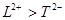
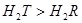
 溶液反应
溶液反应查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:HClO4>H2SO4>H3PO4 | B.稳定性:H2S>HCl>HBr>HI |
| C.碱性:KOH<NaOH<LiOH | D.熔点:SiO2>Na >NaCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Z是海水中含量最高的金属元素,W是地壳中含量最多的金属元素 |
| B.X、M两元素氢化物的稳定性:X<M |
| C.Z和W的氧化物均可做耐高温材料,M的氧化物可做太阳能电池 |
| D.X、W的最高价氧化物的水化物间反应生成一种可净水的化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com