
�����£�Ũ�Ⱦ�Ϊ0.1 mol/L��4����ҺpH���£�
| ���� | Na2CO3 | NaHCO3 | Na2SiO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.3 |
�����ϱ����ݻش�
��1�������ӷ���˵����ҺNaClO��Һ�Լ��Ե�ԭ��
��2�������£���ͬ���ʵ���Ũ�ȵ�����ϡ��Һ����������ǿ���ǣ�����ţ� ��
a��H2SiO3 b��HClO c��H2CO3
��3���û�ѧ����ͱ�Ҫ�����ֽ����ȵ�Na2CO3��Һȥ����������ǿ��ԭ�� ��
��4����������ˮ�д������Ũ�ȣ�������ˮ�м����ϱ��е������ǣ��ѧʽ�� ���û�ѧƽ���ƶ���ԭ��������ԭ�� ��
 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ���������������ȷ����(����)
A������������ȼ�գ�����ʻ�ɫ��������ɫ����
B��������������ȼ�գ�������ɫ���棬ͬʱ��������
C����Ͷ��ˮ�У�������ˮ�ײ��ۻ���С���������ݲ���
D������ͨ����ɫʯ����Һ�У���Һ�ȱ�����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪A��B��C��D��E����Ԫ�ص�ԭ������������������Aԭ����������������������������ԭ��������ȣ�Bԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�����������p�����������������Dԭ��L���Ӳ�����2�ԳɶԵ��ӣ�E��ԭ�Ӻ�����3������Ҹ��������ȫ��״̬������д���пհס�
��1��EԪ�ػ�̬ԭ�ӵĺ�������Ų�ʽΪ_________________��
��2��B��C��D����Ԫ�صĵ�һ��������ֵ��С�����˳��Ϊ_____________����Ԫ�ط��ţ�����ԭ��Ϊ_____________________��
��3��B2A4����Ҫ�Ļ���ʯ�ͻ���ԭ�ϡ�B2A4������Bԭ�ӹ�����ӻ�����Ϊ________��
 1 mol B2A4�����к�__________mol �Ҽ���
1 mol B2A4�����к�__________mol �Ҽ���
��4����֪D��E���γɾ�����ͼ��ʾ�����ֻ����������Ļ�ѧʽ����Ϊ_________����Ϊ___________������ʱ������ת��Ϊ�ҵ�ԭ��Ϊ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���У���ȷ����
A��������ˮ�ĵ����һ����ǿ�����
B��������ˮ�ĵ����һ�����������
C�����������ˮ��Һ�еĵ�������ǿ����
D��ǿ�����ˮ��Һ�ĵ�������һ����������ʵ�ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ij���淴Ӧ���ܱ������н��У�
A(g)+2B(g) 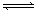 3C(g)+D(s)�����ȷ�Ӧ������ͼ������b����һ�������¸÷�Ӧ�Ĺ��̣���ʹ����b��Ϊ����a���ɲ�ȡ�Ĵ�ʩ��
3C(g)+D(s)�����ȷ�Ӧ������ͼ������b����һ�������¸÷�Ӧ�Ĺ��̣���ʹ����b��Ϊ����a���ɲ�ȡ�Ĵ�ʩ��
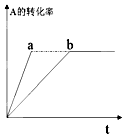
A������A��Ũ�� B�������������ݻ�
C��������� D�������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������л���ṹ��������ص������������(����)
A����������к����Ȼ�������NaHCO3��Һ��Ӧ����CO2
B�������ʺ���֬�����ڸ߷��ӻ����һ�������¶���ˮ��
C�������������Ӧ����һ�ȼ����뱽�����ᷴӦ�����������ķ�Ӧ������ͬ
D��������ʹ������Ȼ�̼��Һ��ɫ��˵����������û������ϩ���������Ƶ�̼̼˫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ�У�����ȡ����Ӧ����(����)
��CH3CH===CH2��Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
��CH3CH2OH CH2===CH2����H2O
CH2===CH2����H2O
��CH3COOH��CH3CH2OH
CH3COOCH2CH3��H2O
��C6H6��HNO3 C6H5NO2��H2O
C6H5NO2��H2O
A���٢ڡ����������� B���ۢ�
C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ����ƿ������ֽ�۳ɵ�ֽ������������һ����Һ��ͨ��ij�������ʵ������Ԥ���ֽ������ɫ�仯��һ�µ���(����)

| A | B | C | D | |
| ����Һ | ��̪ | ��ɫʯ�� | �����ظ���� | �ữ�� KI������ |
| ͨ������� | NH3 | Cl2 | CH3CH2OH(g) | O3 |
| Ԥ�����ɫ�仯 | ��Ϊ��ɫ | ������ɫ | �����Ա仯 | ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ijϡ�����ϡ����Ļ����Һ200 mL��ƽ���ֳ����ݡ�������һ��������ͭ�ۣ�������ܽ�19.2 g(��֪����ֻ����ԭΪNO����)������һ�����������ۣ�������������������������ӵı仯����ͼ��ʾ�����з��������������( )
ijϡ�����ϡ����Ļ����Һ200 mL��ƽ���ֳ����ݡ�������һ��������ͭ�ۣ�������ܽ�19.2 g(��֪����ֻ����ԭΪNO����)������һ�����������ۣ�������������������������ӵı仯����ͼ��ʾ�����з��������������( )
A��H2SO4Ũ��Ϊ4 mol��L-1
B��OA�β�������NO��AB�εķ�ӦΪ
Fe+2Fe3+=3Fe2+��BC�������
C���ڶ�����Һ����������ΪFeSO4
D���������NO3-���ʵ���Ϊ0.2mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com