
| V |
| Vm |
| m |
| n |
| m |
| M |
| 1.12L |
| 22.4L/mol |
| 1.4g |
| 0.05mol |
| 5.6g |
| 28g/mol |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中存在大量单质硅 | ||||
| B、硅元素是形成地壳的主要元素,在地壳中的含量占第一位 | ||||
C、纯硅可以通过下列反应制得:SiO2+2C
| ||||
| D、单晶硅是良好的半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
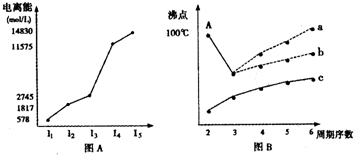
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl、BaCl2、AgNO3 |
| B、Ba(NO3)2、AgNO3、HNO3 |
| C、HNO3、Ba(NO3)2、AgNO3 |
| D、酚酞、Ba(NO3)2、AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成1mol Fe3O4,反应转移的电子总数为3mol | ||
| B、Fe2+和S2O32-都是还原剂 | ||
C、1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为
| ||
| D、x=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com