
| A、2个 | B、3个 | C、4个 | D、5个 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| A、1mol H2和0.5mol O2所具有的总能量低于1mol气态H2O所具有的总能量 | ||
| B、氢气跟氧气反应生成水的同时吸收能量 | ||
C、1mol H2跟
| ||
| D、2mol H2(g)跟1mol O2(g)反应生成2mol H2O(g)释放能量490kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | K2CO3 | KHCO3 | K2SO3 |
| 质量(kg) | 55.2 | 120.0 | 63.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液滴加过量的氨水:Al3++4NH3?H2O═AlO2-+4NH4++H2O |
| B、硫酸和氢氧化钡溶液反应:H++SO42-+OH-+Ba2+═BaSO4↓+H2O |
| C、向氯化钙溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
| D、向氢氧化铁胶体中滴加足量HI溶液:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| 电离平衡常数K (25℃) |
K=4.93×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
K=3.53×10-4 |
| A、NaCN溶液中通入少量CO2:CN-+H2O+CO2→HCN+HCO3- |
| B、Na2CO3溶液中通入少量HF:CO32-+2HF→2F-+CO2+H2O |
| C、25℃,等浓度的NaCN和NaF溶液中pH值前者大于后者 |
| D、中和等体积、等pH的HCN和HF消耗NaOH的量前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、合成聚乙烯塑料: | |||
B、溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH
| |||
C、向稀苯酚溶液中滴加少量浓溴水:2 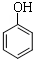 +3Br2→2 +3Br2→2 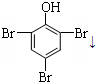 ↓ ↓ | |||
D、实验室制乙烯:CH3CH2OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、当有0.2 mol电子转移时,a电极产生2.24 L H2 |
| B、b电极上发生的电极反应式为2H++2e-═H2↑ |
| C、d电极上发生的电极反应式为O2+4H++4e-═2H2O |
| D、d电极上进行氧化反应,B池中的H+可以通过隔膜进入A池 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com