
| 弱酸 | 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| 电离平衡常数K (25℃) |
K=4.93×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
K=3.53×10-4 |
| A、NaCN溶液中通入少量CO2:CN-+H2O+CO2→HCN+HCO3- |
| B、Na2CO3溶液中通入少量HF:CO32-+2HF→2F-+CO2+H2O |
| C、25℃,等浓度的NaCN和NaF溶液中pH值前者大于后者 |
| D、中和等体积、等pH的HCN和HF消耗NaOH的量前者小于后者 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

| 一定条件 |
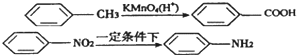
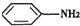 (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)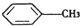 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物.
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
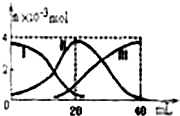 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,横坐标表示加入NaOH的体积).根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,横坐标表示加入NaOH的体积).根据图示判断,下列说法正确的是( )| A、当V(NaOH)=40mL时,c(Na+)+c(H+)=2c(A2-)+c(OH-) |
| B、当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C、滴加过程中当溶液呈中性时,V(NaOH)<20mL |
| D、HA-的电离程度小于水解程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、该装置能将电能转化为化学能 |
| B、活性炭为正极,其电极反应式为:2H++2e-═H2↑ |
| C、电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
| D、装置内总反应方程式为:4Al+3O2+6H2O═4Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、612C和613C |
| B、O2和O3 |
| C、(CH3)2CHCH2CH3和C(CH3)4 |
| D、H2C(CH3)2和CH3CH2 CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液的pH小于7 |
| B、c(HF)+c(F-)=0.2 mol?L-1 |
| C、c(HF)<c(F-) |
| D、c(F-)+c(OH-)=0.1 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、打算制成小包装用于糕点的脱氧剂 |
| B、利用反应放出热量的原理制成暖宝宝 |
| C、调整电池结构,可降低温度,可用于延长糕点保质期 |
| D、正极的电极反应为:2H2O+O2+4e-=4OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com