

| A、该装置能将电能转化为化学能 |
| B、活性炭为正极,其电极反应式为:2H++2e-═H2↑ |
| C、电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
| D、装置内总反应方程式为:4Al+3O2+6H2O═4Al(OH)3 |


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
| 3 |
| 5 |
| 离子 | Cu2+ | H+ | CI- | SO42- |
| c/mol?L-1 | 0.5 | 2 | 2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| 电离平衡常数K (25℃) |
K=4.93×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
K=3.53×10-4 |
| A、NaCN溶液中通入少量CO2:CN-+H2O+CO2→HCN+HCO3- |
| B、Na2CO3溶液中通入少量HF:CO32-+2HF→2F-+CO2+H2O |
| C、25℃,等浓度的NaCN和NaF溶液中pH值前者大于后者 |
| D、中和等体积、等pH的HCN和HF消耗NaOH的量前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含1mol NH3?H2O |
| B、含NH3、NH4+之和为1mol |
| C、只含有1mol NH3 |
| D、NH3、NH3?H2O、NH4+之和为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、合成聚乙烯塑料: | |||
B、溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH
| |||
C、向稀苯酚溶液中滴加少量浓溴水:2 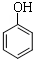 +3Br2→2 +3Br2→2 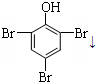 ↓ ↓ | |||
D、实验室制乙烯:CH3CH2OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用相同浓度的HNO3溶液中和,硝酸体积小于氨水时,溶液可能呈中性 |
| B、温度不变,加水稀释后溶液中c(NH4+)?c(OH-)不变 |
| C、加水稀释后,溶液中导电粒子的数目减少 |
| D、其溶液的pH=13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
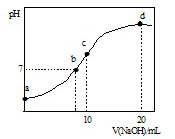 常温下,向20.00mL 0.1000mol?L-1 (NH4)2SO4溶液中逐滴加入0.2000mol?L-1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如右图所示(不考虑挥发).下列说法正确的是 ( )
常温下,向20.00mL 0.1000mol?L-1 (NH4)2SO4溶液中逐滴加入0.2000mol?L-1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如右图所示(不考虑挥发).下列说法正确的是 ( )| A、点a所示溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+) |
| B、点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C、点c所示溶液中:c(SO42-)+c(H+)=c(NH3?H2O )+c(OH-) |
| D、点d所示溶液中:c(SO42-)>c(NH3?H2O )>c(OH-)>c(NH4+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com