
【题目】向Cu和Fe混合物中加入一定量的稀HNO3,充分反应后,剩余固体为ag再加入一定量的稀H2SO4,最后剩余固体为bg.则下列说法正确的是
A.b>aB.b=aC.b<aD.b≤a
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A. a g C2H4和C3H6的混合物所含原子总数为![]()
B. 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
C. 标准状况下,22.4 L H2O含有的分子数为 NA
D. 物质的量浓度为0.5 mol·L1的MgCl2溶液中,含有Cl个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氨的水溶液显弱碱性,其原因为___________________(用离子方程式表示), 0.1 molL-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度__________(填“增大”或“减小”);
(2)25℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=___________________;
②0.10molL-1Na2SO3溶液中离子浓度由大到小的顺序为___________________;
③H2SO3溶液和NaHCO3溶液反应的离子方程式为___________________;
(3)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知Ksp(AgCl)=1.8×10-10,若向5mL0.018molL-1的AgNO3溶液中加入5mL0.020molL-1的盐酸,混合后溶液中的Ag+的浓度为______molL-1,pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)![]() cC(g)。反应过程中,物质A的体积分数
cC(g)。反应过程中,物质A的体积分数
和C的体积分数随温度(T)的变化曲线如图所示。下列说法正确的是
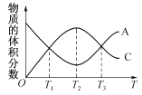
A.该反应在T1、T3温度时达到化学平衡 B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应 D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 标准状况下,22.4L水中所含的分子数约为6. 02×1023个。
B. 1 mol Cl2中含有的原子数为NA
C. 标准状况下,4.48L氧气和氮气的混合物含有的分子数约为1.204×1023个。
D. 从1L 0.5 mol/L NaCl溶液中取出100ml,剩余溶液中NaCl的物质的量浓度为0.45 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是

A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.吸收塔中发生的反应有SO2+H2O![]() H2SO3
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,SO42-浓度与海水相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是
A. 乙烯通入酸性高锰酸钾溶液中
B. 苯与液溴混合后撒入铁粉
C. 在镍做催化剂的条件下,苯与氢气反应
D. 乙烯通入溴水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机高分子合成材料的出现是材料发展史上的一次重大突破,下列属于有机高分子合成材料的一组是( )
①家用保鲜袋 ②不锈钢 ③淀粉 ④尼龙布 ⑤汽车轮胎
A.①④⑤B.②③④C.②③⑤D.只有①⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com