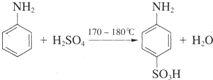
(2010?江苏二模)CuCl和CuCl
2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
已知:①CuCl可以由CuCl
2用适当的还原剂如SO
2、SnCl
2等还原制得:2Cu
2++2Cl
-+SO
2+2H
2O
2CuCl↓+4H
++SO
42-2CuCl
2+SnCl
2═2CuCl↓+SnCl
4②CuCl
2溶液与乙二胺(H
2N-CH
2-CH
2-NH
2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为
1s22s22p63s23p63d104s1
1s22s22p63s23p63d104s1
,H、N、O三种元素的电负性由大到小的顺序是
O>N>H
O>N>H
.
(2)SO
2分子的空间构型为
V形
V形
,与SnCl
4互为等电子体的一种离子的化学式为
SO42-、SiO44-
SO42-、SiO44-
.
(3)乙二胺分子中氮原子轨道的杂化类型为
sp3杂化
sp3杂化
,乙二胺和三甲胺[N(CH
3)
3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键
乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键
.
(4)②中所形成的配离子中含有的化学键类型有
abd
abd
.a.配位键 b.极性键 c.离子键 d.非极性键
(5)CuCl的晶胞结构如下图所示,其中Cl原子的配位数为
4
4
.