
【题目】化学与生产生活密切相关。下列说法错误的是
A. 纤维素是多糖,可以作人类的营养物质
B. 利用高纯度单质硅可以制成太阳能光伏电池
C. 制作宇宙飞船的玻璃纤维和玻璃的成分相同
D. C1O2可用作自来水消毒剂
科目:高中化学 来源: 题型:
【题目】工业上常用软锰矿(主要成分为MnO2)制备KMnO4,,其流程如下所示:

(1)将原料粉碎后,通人空气,加热熔融时,发生反应的化学方程式为_______________。
(2)软锰矿中除了含有MnO2,还含有Fe2O3、MgO、Al2O3、SiO2等杂质,这些杂志会导致KOH消耗量______
(填“偏高”或“偏低”)。
(3)上述过程中可以循环使用的物质有MnO2和_____________(写化学式)。
(4)反应a的化学方程式为________________。
(5)操作I的名称为_________,操作II利用KMnO4和K2CO3溶解性的差异,采取________(填操作方法名称)、趁热过滤得到KMnO4,粗晶体。粗晶体洗涤后得到纯净的晶体。证明晶体已经洗涤干净的操作是______。
(6)某工厂排放的废水中含有Mn2+、Ca2+、Mg2+(阴离子为SO42-),若想将Mn2+回收利用,可利用以下流程:

已知:

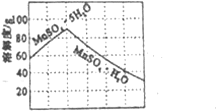
物质X应选用__________(由一种阳离子和一种阴离子组成,填化学式);根据溶解度曲线可知,采用蒸发浓缩、趁热过滤操作时需控制的温度最适宜为___________(填序号)。
①20℃ ②40℃ ③80℃ ④120℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】课外小组的同学利用下图装置研究铜与稀硝酸的反应。

(1)铜与稀硝酸反应的离子方程式________________________________________。
(2)实验过程中水槽中的集气瓶收集到无色气体,甲同学由此认为铜与稀硝酸反应生成了NO。乙同学认为上述理由不完备,原因是________________________________________(用化学方程式表示)。
(3)同学们经过讨论,决定改用装置B进行反应,实验步骤①~③如下图所示。

步骤③拔去注射器的橡胶帽,拉动活塞吸入少量的空气后,迅速盖上橡胶帽。如果观察到____________________的现象,就能证明铜与稀硝酸反应生成了NO。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮在自然界中的转化是一个复杂的过程,涉及到地球上生物的方方面面。
(1)下列关于自然界中氮循环(如下图)的说法不正确的是(______)

A.氮元素均被氧化
B.工业合成氨属于人工固氮
C.含氮无机物和含氮有机物可相互转化
D.碳、氢、氧三种元素也参与了氮循环
(2)汽车尾气中的NO和NO2,是大气污染的物质。
①写出NO造成酸雨的两个化学反应方程式____________________。
②在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为无毒气体,该反应的化学反应方程式______________________________。
③用O2-NaOH吸收法可以除去烟道气中的NO2。反应的化学方程式是______________________________。
(3)用化学方程式表达工业上以NH3为原料生产HNO3的第一步______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物结构、性质的分析正确的是
A. 2-甲基丙烷也称为异丙烷
B. 油脂和蛋白质都属于高分子化合物
C. 丙烯、苯分子的所有原子均在同一平面内
D. 葡萄糖与果糖互为同分异构体,均能与金属钠反应产生H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用硝酸为原料生产亚硝酸钠的工艺流程如下,等物质的量的NO和NO2恰好能被Na2CO3溶液在吸收塔中完全吸收生成NaNO2。

(1)吸收塔中发生反应的化学方程式是____________________。
(2)分解塔中需要严格控制硝酸的浓度,目的是______________________________。
(3)向母液中加入硝酸,发生反应3NaNO2+2HNO3=3NaNO3+2NO↑+H2O,经结晶可制得副产品NaNO3。对该过程中产生的NO的处理方法是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法正确的是
A. SO2、CO2、NO2都是可形成酸雨的气体
B. 天然纤维、人造纤维、合成纤维的组成元素相同
C. 地沟油不宜食用,可以分馏提取汽油,做汽车的燃料
D. 《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
①C(s)+O2(g)===CO2(g) ΔH1 C(s)+![]() O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+![]() O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
A. ① B. ④ C. ②③④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。
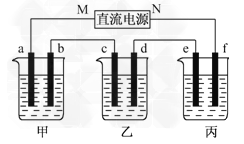
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为____________________极;
②电极b上发生的电极反应为____________________;
③列式计算电极b上生成的气体在标准状况下的体积:________________;
④电极c的质量变化是__________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:甲溶液______________________________;乙溶液______________________________;丙溶液______________________________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么? ________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com