
����Ŀ����ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100 g 5.00%��NaOH��Һ��������CuSO4��Һ��100 g 10.00%��K2SO4��Һ���缫��Ϊʯī�缫��
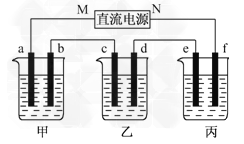
(1)��ͨ��Դ������һ��ʱ���ñ���K2SO4Ũ��Ϊ10.47%������c�缫�������ӡ��ݴ˻ش����⣺
����Դ��N��Ϊ____________________����
���缫b�Ϸ����ĵ缫��ӦΪ____________________��
����ʽ����缫b�����ɵ������ڱ�״���µ������________________��
���缫c�������仯��__________g��
�����ǰ�����Һ���ᡢ���Դ�С�Ƿ����仯��������ԭ����Һ______________________________������Һ______________________________������Һ______________________________��
(2)�����������ͭȫ����������ʱ����ܷ�������У�Ϊʲô�� ________________________________________��
���𰸡� �� 4OH����4e��===2H2O��O2�� ˮ���ٵ�������100g��(1��![]() )��4.5g ����O2�����
)��4.5g ����O2����� ![]() ��
��![]() ��22.4L��mol-1=2.8L 16 ����������Ϊ����ˮ�����٣���Һ��NaOHŨ������ ����������Ϊ������OH������O2����Һ��H������Ũ������ ����Դ�Сû�б仯����ΪK2SO4��ǿ��ǿ���Σ�Ũ�����Ӳ�Ӱ����Һ������� �ܼ������У���ΪCuSO4��Һ��ת��ΪH2SO4��Һ����ӦҲ�ͱ�Ϊˮ�ĵ�ⷴӦ
��22.4L��mol-1=2.8L 16 ����������Ϊ����ˮ�����٣���Һ��NaOHŨ������ ����������Ϊ������OH������O2����Һ��H������Ũ������ ����Դ�Сû�б仯����ΪK2SO4��ǿ��ǿ���Σ�Ũ�����Ӳ�Ӱ����Һ������� �ܼ������У���ΪCuSO4��Һ��ת��ΪH2SO4��Һ����ӦҲ�ͱ�Ϊˮ�ĵ�ⷴӦ
��������(1)���ұ���c�������ӣ�˵��Cu������c�缫�ϣ������Ǵ�b-c�ƶ���M�Ǹ�����NΪ������
������ΪNaOH���൱�ڵ��H2O������b��Ϊ������OH-�ŵ磬��4OH--4e-=2H2O+O2����
������ΪK2SO4���൱�ڵ��ˮ�������ˮ������Ϊx���ɵ��ǰ��������������У�100��10%=(100-x)��10.47%����x=4.5g����Ϊ0.25mol���ɷ���ʽ2H2+O2�T2H2O��֪������2molH2O��ת��4mol���ӣ�����������Ӧ��ת��0.5mol���ӣ�������O2Ϊ0.5/4=0.125mol������µ����Ϊ0.125��22.4=2.8L��
��������·�Ǵ����ģ�����ÿ���ձ��еĵ缫��ת�Ƶ���������ȵģ����ݵ缫��Ӧ��Cu2++2e-=Cu����֪ת��0.5mol�������ɵ�m(Cu)= ![]() ��64=16g��
��64=16g��
�������൱�ڵ��ˮ����NaOH��Ũ������pH�����������ΪCu2+�ŵ磬����ΪOH-�ŵ磬��ⷽ��ʽΪ��2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4������H+���࣬��pH��С������Ϊ���ˮ������K2SO4���ԣ���pH�������䣻
2Cu+O2��+2H2SO4������H+���࣬��pH��С������Ϊ���ˮ������K2SO4���ԣ���pH�������䣻
(2)��ͭȫ������ʱ����Һ�����е�������ᣬ���Լ�����⣬�ʴ�Ϊ�����ԣ� ͭȫ�����������Լ������H2SO4���е��Һ���ɵ�⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����������������ء�����˵���������
A. ��ά���Ƕ��ǣ������������Ӫ������
B. ���øߴ��ȵ��ʹ�����Ƴ�̫���ܹ�����
C. ��������ɴ��IJ�����ά�Ͳ����ijɷ���ͬ
D. C1O2����������ˮ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����������������ء�����˵����ȷ����
A. ��ȼ��Al(OH)3���ȷֽ�ʱ�ų�����
B. ��˿�����ڡ�������Ҫ�ɷ־�Ϊ������
C. ��֬�ڳ�����������������ø�Ϳ����е��������ûᷢ�����
D. ��̫���ܵ����ͭпԭ��ع���ʱ���ɻ�ѧ��ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������м���ڹ�����ϡ������ټ����������ʣ�����Fe3+���ɵ���
A. ����п B. ��ˮ C. �Ȼ�ͭ D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Է�������Ϊ92��ij������X��һ����Ҫ���л�����ԭ�ϣ��о���������Ϊ��ʼԭ����Ƴ�����ת����ϵͼ�����ֲ���ϳ�·�ߡ���Ӧ������ȥ��������A��һ�ȴ��H��һ�ֹ��ܸ߷��ӣ��������ΪC7H5NO��
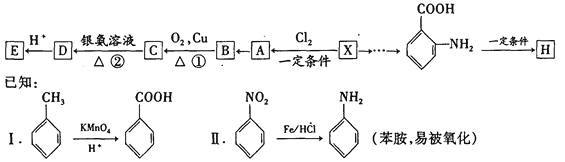
�������ѧ֪ʶ�뱾��������Ϣ�ش��������⣺
��1��X������Ϊ____________, B�й�����Ϊ____________��
��2����Ӧ�ٵķ�Ӧ������____________
��3��H�Ľṹ��ʽ��____________��
��4����Ӧ�ڵĻ�ѧ����ʽ��____________��
��5�� E�ж���ͬ���칹�壬�����ܷ���������Ӧ�ķ����廯���ﹲ��____�֣����������칹����д���ں˴Ź����������ܳ����������������֮��Ϊl:1:2:2��ͬ���칹��Ľṹ��ʽΪ____________��
��6�����úϳ�����ͼ��ʾ����X����������ϳ�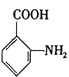 ������ķ���____________��������3������
������ķ���____________��������3������
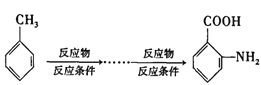
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ʊ������Ȼ���ʱ���������ַ���:������������ֱ�ӻ����Ƶ��������������ᷴӦ�Ƶã����������ַ��������Ƶõ��Ȼ�����
A. AlCl3 B. FeCl3 C. FeCl2 D. CuCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҩ��ϳ����л��ϳɵ���ҪӦ�ã�����·�߿����ںϳ�һ�������{Ѫѹ�����IJ���ҩ�F�����Իش��������⣺
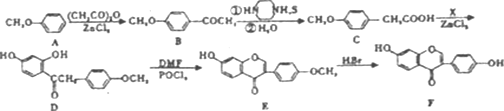
(1)A����B�ķ�Ӧ����Ϊ_______________��
(2)C��X����ȡ����Ӧ����D��ͬʱ����H2O���ɣ���X������Ϊ______________��д���÷�Ӧ�Ļ�ѧ����ʽ________________________��
(3)������F�еĺ�����������____________������������ƣ���
(4)�л���Y��B��ͬ���칹�壬��Y��������������д��T�Ľṹ��ʽ___________��
�����ڷ����廯�����FeCl3��Һ������ɫ��Ӧ��
����������Cu(OH)2��Ӧ����ש��ɫ������
��������ˮ��Ӧ���ɳ�������1mol Y������2mol Br2��
�ܷ�������4�ֲ�ͬ��ѧ�������⡣
(5)���������ϳ�·�ߣ��������һ����![]() ��������Ϊԭ���Ʊ�
��������Ϊԭ���Ʊ�![]() �ĺϳ�·��(���Լ���ѡ)________________��
�ĺϳ�·��(���Լ���ѡ)________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 4 molA�����3molB������2L�������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g��![]() 2C��g��, ���� 2 s���� C��Ũ��Ϊ 0.6 molL-1���������м���˵����
2C��g��, ���� 2 s���� C��Ũ��Ϊ 0.6 molL-1���������м���˵����
��������A ��ʾ��Ӧ��ƽ������Ϊ 0.3 molL-1s-1
������ B�����������40%
��2 s ʱ���� A ��ת����Ϊ30��
��2 s ʱ���� B ��Ũ��Ϊ 1.0 molL-1
������ȷ����
A. �٢� B. �ڢ� C. �٢� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I. ������ʵд�����з�Ӧ���Ȼ�ѧ����ʽ��
�� ��25�桢101kPa��,1g�״�CH3OHȼ������CO2��Һ̬ˮʱ����22.68kJ��
���ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ__________________��
�� ��������N2��O2��ȫ��Ӧ,ÿ����23��NO2��Ҫ����16.95kJ����_____________��
II. ��˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ
��Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) ��H= �D24.8 kJ.mol -1
��3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) ��H= �D47.2 kJ.mol -1
��Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) ��H= +640.5 kJ.mol -1
д��CO���廹ԭFeO����õ�Fe�����CO2������Ȼ�ѧ��Ӧ����ʽ________________��
III����֪��Ӧ 2HI��g��=H2(g) + I2(g)�ġ�H=+11kJ��mol-1��1molH2��g���� 1molI2��g�������л�ѧ������ʱ�ֱ���Ҫ���� 436KJ��151KJ ���������� 1molHI��g�������л�ѧ������ʱ�����յ�����Ϊ______________kJ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com