
| X | Z | |
| Y |
| A. | 原子序数由大到小为 Z>Y>X | |
| B. | 氢化物最稳定的元素为Y | |
| C. | X的最高价氧化物对应的水化物的稀溶液能与铜发生反应 | |
| D. | 原子半径由大到小的顺序为 Z>Y>X |
分析 由短周期元素的位置可知,X、Z处于第二周期,Y处于第三周期,由于X的最高正价与最低负价绝对值的和为8,最高正价与负价的代数和为2,可知X的最高正价为+5,故其最外层有5个电子,则X为N、Y为S,Z为F,结合元素周期律与元素化合物性质解答.
解答 解:由短周期元素的位置可知,X、Z处于第二周期,Y处于第三周期,由于X的最高正价与最低负价绝对值的和为8,最高正价与负价的代数和为2,可知X的最高正价为+5,故其最外层有5个电子,则X为N、Y为S,Z为F.
A.原子序数由大到小为 Y>Z>X,故A错误;
B.F元素非金属性最强,故HF最稳定,故B错误;
C.X的最高价氧化物对应的水化物为硝酸,稀硝酸溶液能与铜发生反应,故C正确;
D.原子半径由大到小的顺序为 Y>X>Z,故D错误,
故选:C.
点评 本题考查结构性质位置关系应用,注意对元素周期律的理解掌握,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 10 L 0.05mol•L-1Ba(OH)2溶液与10 L 0.05mol•L-1 H2SO4反应时的反应热是中和热 | |
| B. | 由2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ•mol-1知,该反应的反应热为571.6 kJ•mol-1 | |
| C. | 由2H2(l)+O2(l)=2H2O(g)△H=-482.6 kJ•mol-1知,H2的燃烧热为482.6 kJ•mol-1 | |
| D. | 由C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2221.5 kJ•mol-1知,气体C3H8的燃烧热为2221.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在50mL量筒中配制0.1000mol•L-1碳酸钠溶液 | |
| B. | 仅用烧杯、量筒、玻璃棒就可以配制100mL0.1000mol•L-1K2Cr2O7溶液 | |
| C. | 用100mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管和pH=1的盐酸配制100mLpH=2的盐酸 | |
| D. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余液体吸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与稀盐酸的反应 | B. | 氢氧化钡晶体与氯化铵晶体的反应 | ||
| C. | 甲烷在氧气中的燃烧反应 | D. | 灼热的碳与二氧化碳的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1﹕3 | B. | 1﹕2 | C. | 1﹕1 | D. | 2﹕1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知在酸性条件下有以下反应:①2BrO3-+I2═2IO3-+Br2;②2IO3-+10Br-+12H+═I2+5Br2+6H2O.
已知在酸性条件下有以下反应:①2BrO3-+I2═2IO3-+Br2;②2IO3-+10Br-+12H+═I2+5Br2+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

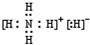 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 27.5 mL | B. | 17.5 mL | C. | 15 mL | D. | 3 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com