


 具有相同的含氮六元杂环和官能团的同分异构体共有_________ 种(包含本身。已知含氮六元杂环与苯环结构相似)。
具有相同的含氮六元杂环和官能团的同分异构体共有_________ 种(包含本身。已知含氮六元杂环与苯环结构相似)。 和
和 为原料,合成
为原料,合成 ,合成过程中无机试剂任选;合成路线流程图示例如下:
,合成过程中无机试剂任选;合成路线流程图示例如下: 
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:








| 次硫酸 |
| ℃170 |
| Br |


查看答案和解析>>
科目:高中化学 来源: 题型:

 Ⅱ.
Ⅱ.






 具有相同的含氮六元杂环和官能团的同分异构体共有
具有相同的含氮六元杂环和官能团的同分异构体共有 和
和 为原料,合成
为原料,合成 ,合成过程中无机试剂任选;合成路线流程图示例如下:
,合成过程中无机试剂任选;合成路线流程图示例如下:| 浓硫酸 | 170℃ |
 BrH2C-CH2Br.
BrH2C-CH2Br.

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
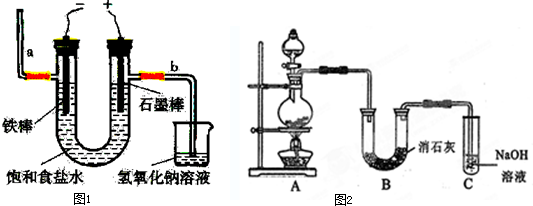
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2010年高考试题--理综化学(浙江卷)解析版 题型:实验题
(15分)一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4·H2O是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:

相关信息如下:
①[Cu(NH3)4]SO4·H2O在溶液中存在以下电离(解离)过程:
 [Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++
[Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++ +H2O
+H2O
[Cu(NH3)4]2+ Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇·水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:
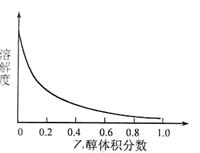

请根据以下信息回答下列问题: 图3
(1)方案1的实验步骤为:
a. 加热蒸发 b. 冷却结晶 c. 抽滤 d. 洗涤 e. 干燥
①步骤1的抽滤装置如图3所示,该装置中的错误之处是 ;抽滤完毕或中途停止抽滤时,应先 ,然后 。
②该方案存在明显缺陷,因为得到的产物晶体中往往含有 杂质,产生该杂质的原因是 。
(2)方案2的实验步骤为:
a. 向溶液C中加入适量 ,b. ,c. 洗涤,d. 干燥
①请在上述内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是 。
A. 乙醇 B. 蒸馏水 C. 乙醇和水的混合液 D. 饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com