
【题目】室温下,一种气态烷烃和一种气态烯烃的混合物9克,其密度是相同条件下H2密度的11.25倍.当混合物通过足量的溴水时,溴水增重4.2克,则这两种气态烃是( )
A.C2H6和C2H4
B.CH4和C3H6
C.CH4和C2H4
D.CH4和C4H8
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是 ( )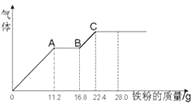
A.混合酸中HNO3物质的量浓度为1mol/L-1
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+ , BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.原混合酸中H2SO4物质的量浓度为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g)3Z(g),平衡时,X,Y,Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X,Y,Z的体积分数不变.下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中,不正确的是
A. 胶体是一种介稳体系 B. 胶体中分散质粒子的直径小于1 nm
C. 利用丁达尔效应可以区分溶液和胶体 D. 用滤纸能分离胶体和悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图.下列对该化合物叙述正确的是( ) 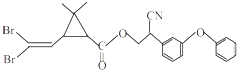
A.属于芳香烃
B.属于卤代烃
C.在酸性条件下不水解
D.在一定条件下可以发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H1=﹣53.7kJmol﹣1 Ⅰ
CO2(g)+H2(g)CO(g)+H2O(g)△H2 Ⅱ
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性;转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为﹣283.0kJmol﹣1和﹣285.8kJmol﹣1 .
②H2O(1)═H2O(g)△H3=44.0kJmol﹣1
请回答(不考虑温度对△H的影响):
(1)反应I的平衡常数表达式K=;反应Ⅱ的△H2=kJmol﹣1 .
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有 .
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大 CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是 .
(4)在如图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程﹣能量”示意图.
(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在极,该电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示.A元素的某种同位素原子没有中子,D元素的原子序数是C的2倍,E是短周期主族元素中半径最大的元素.下列说法不正确的是( )
A.简单离子的半径大小关系:B>C>E
B.D,E两种元素形成的化合物,可能含有离子键和共价键
C.A,B,C三种元素形成的化合物,晶体类型一定相同
D.B,D分别和C形成的化合物,都有可能使溴水或品红溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1000 mL某待测溶液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种如下表,现进行如下实验操作(每次实验所加试剂均过量):
阳离子 | K+、NH |
阴离子 | Cl-、Br-、CO |
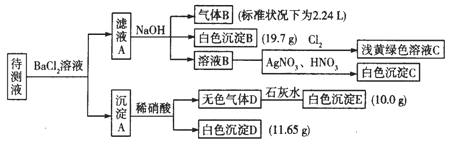
(1)写出生成白色沉淀B的离子方程式:_________。
(2)待测液中肯定不存在的阳离子是_______。
(3)若无色气体D是单一气体:判断原溶液中K+是否存在____(填“是”或“否”),若存在,求其物质的量浓度的最小值,若不存在,请说明理由:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)用作香料的原料,它可由A合成得到( ) 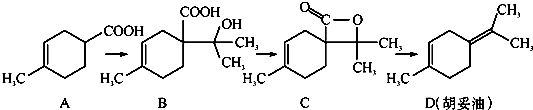
A.从B到C的反应是消去反应
B.D分子中所有碳原子一定共面
C.等物质的量的B分别与足量的Na、NaHCO3反应,产生的气体的物质的量前者大于后者
D.若A是由2﹣甲基﹣1,3﹣丁二烯和丙烯酸(CH2=CHCOOH)加热得到的,则该反应的类型属于加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com