
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g)3Z(g),平衡时,X,Y,Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X,Y,Z的体积分数不变.下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4molL﹣1
【答案】D
【解析】解:A.平衡时,X、Y、Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X、Y、Z的体积分数不变,说明反应前后气体计量数之和不变,所以m=2,故A正确;
B.平衡常数只与温度有关,温度不变,平衡常数不变,所以两次平衡的平衡常数相同,故B正确;
C.设第一次达到平衡状态时X参加反应的物质的量为amol,
X(g)+ | 2Y(g) | 3Z(g) | ||
开始(mol) | 1 | 2 | 0 | |
转化(mol) | a | 2a | 3a | |
平衡(mol) | 1﹣a | 2﹣2a | 3a |
相同条件下,气体的体积与物质的量成正比,所以其体积分数等于其物质的量分数,即(1﹣a):(2﹣2a):3a=30%:60%:10%,所以a=0.1,则参加反应的△n(X)=0.1mol、△n(Y)=0.2mol,
转化率= ![]() ,
,
X的转化率= ![]() =10%,Y的转化率=
=10%,Y的转化率= ![]() =10%,所以X和Y的转化率之比为1:1,故C正确;
=10%,所以X和Y的转化率之比为1:1,故C正确;
D.该反应的反应前后气体计量数之和不变,第一次反应是按照X、Y的计量数之比来投料,所以第二次平衡与第一次平衡是等效平衡,两次平衡后各物质的含量不变,投入Z后,设Z参加反应的物质的量为3bmol,
X(g)+ | 2Y(g) | 3Z(g) | ||
第一次平衡(mol) | 0.9 | 1.8 | 0.3 | |
加入1molZ | 0.9 | 1.8 | 1.3 | |
转化 | b | 2b | 3b | |
第二次平衡(mol) | 0.9+b | 1.8+2b | 1.3﹣3b |
各物质含量不变,所以(0.9+b):(1.8+2b):(1.3﹣3b)=30%:60%:10%=3:6:1,
b=0.3,n(Z)=(1.3﹣0.9)mol=0.4mol,Z的物质的量浓度= ![]() =0.2mol/L,故D错误;
=0.2mol/L,故D错误;
故选D.
A.平衡时,X、Y、Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X、Y、Z的体积分数不变,说明反应前后气体计量数之和不变;
B.平衡常数只与温度有关,温度不变,平衡常数不变;
C.设第一次达到平衡状态时X参加反应的物质的量为amol,根据转化率= ![]() 进行计算;
进行计算;
D.该反应的反应前后气体计量数之和不变,第一次反应是按照X、Y的计量数之比来投料,所以第二次平衡与第一次平衡是等效平衡,两次平衡后各物质的含量不变,据此解答.


科目:高中化学 来源: 题型:
【题目】下列有关判断的依据正确的是( )
A.电解质:水溶液是否导电
B.原子晶体:构成晶体的微粒是否是原子
C.共价分子:分子中原子间是否全部是共价键
D.化学平衡状态:平衡体系中各组分的物质的量浓度是否相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)溶液中,c(H+)=10﹣x molL﹣1 , c(OH﹣)=10﹣y molL﹣1 , x与y的关系如图1所示. 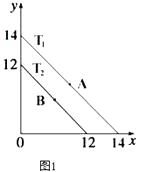
①若从A点到B点,可采取的措施为
②T2℃时,将pH=0的NaHSO4溶液逐滴滴加到pH=2 的醋酸溶液中,则水电离出的c(OH﹣)将(填“增大”、“减小”、“不变”).
③已知:T1℃时,醋酸的电离常数为 1.8×10﹣5 , 则 T1℃时,在 0.5molL﹣1的醋酸溶液中由醋酸电离出的 c(H+)约是水电离出的 c(H+)的倍 .
④T2℃时,将某溶液(此溶液满足 lg[ ![]() ]=10)滴入含 Na+、HS﹣、SO42﹣、K+的溶液中,发生反应的离子方程式为 .
]=10)滴入含 Na+、HS﹣、SO42﹣、K+的溶液中,发生反应的离子方程式为 .
(2)体积均为1mL pH=2的一元酸HA和HB,加水稀释过程中pH与溶液体积关系如图2所示: 
①m的取值为 .
②a点酸的浓度b点酸的浓度(填“>”、“<”、“=”).
③若 m<4,常温下a点到c点的过程中,下列表达式的数据变大的是 .
A.c(A﹣) B.n(H+)n(OH﹣) C. ![]() D.
D. ![]()
(3)已知:25℃时,HCN、H2CO3 的电离平衡常数分别为K=4.9×10﹣10 , K1=4.3×10﹣7、K2=5.6×10﹣11 , 向NaCN溶液中通入少量CO2 , 所发生反应的离子方程式为:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已成为人类社会面临的重大威胁,下列对应关系不正确的是
环境问题 | 主要污染物 | 环境问题 | 主要污染物 | ||
A | 酸雨 | 二氧化硫 | C | 白色污染 | 二氧化硅 |
B | 温室效应 | 二氧化碳 | D | 光化学烟雾 | 二氧化氮 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将22.4L HCl完全溶于1L水中(水的密度近似为1g/mL),溶液的密度为ρ g/cm3 , 溶液的体积为V mL,溶质的质量分数为w,溶质的物质的量浓度为c mol/L.下列叙述中正确的是( )
①w= ![]() ×100% c=1molL﹣1 向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w 所得溶液中含有NA个HCl分子.
×100% c=1molL﹣1 向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w 所得溶液中含有NA个HCl分子.
A.全部
B.①③④
C.①③
D.只有①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度时,向2.0L恒容密闭容器中充入2molSO2和1molO2 , 发生反应:2SO2(g)+O2(g)2SO3(g).经过一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | t1 | t2 | t3 | t4 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A.反应在前t1s的平均速率v(O2)=0.4/t1molL﹣1s﹣1
B.保持其他条件不变,体积压缩到1.0L,平衡常数将增大
C.保持温度不变,向该容器中再充入0.3 molSO2、0.1molO2和0.2molSO3 , 则此时V正>V逆
D.相同温度下,起始时向容器中充入4mol SO3 , 达到平衡时,SO3的转化率大于10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对标准状况下的四种气体的关系从小到大表示不正确的是( )
①6.72L甲烷 ②3.01×1023HCl分子 ③13.6g H2S ④0.2mol NH3 .
A.质量:④<①<③<②
B.密度:①<④<③<②
C.体积:④<①<②<③
D.氢原子数:②<④<③<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( ) 
A.该反应的△H=+91 kJmol﹣1
B.加入催化剂,该反应的△H变小
C.反应物的总能量小于生成物的总能量
D.如果该反应生成液态CH3OH,则△H减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为蒸馏实验装置.
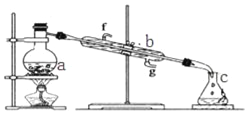
(1)写出下列仪器的名称:a.__ b.__;
(2)实验过程中,需要通冷水,图中的进水方向是__进(填图中字母);
(3)若利用装置分离四氯化碳和酒精的混合物,还缺少的用品是__.
(4)若用装置制蒸馏水,实验时a中除加入少量自来水外,还需加入少量__,其作用是防止暴沸.
II.(5)现需配制0.1molL﹣1NaOH溶液480mL,根据此,回答下列问题:
①配制氢氧化钠溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和__.
②实验时需要称量氢氧化钠__g;
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)__.
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,上下颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④配制0.1molL﹣1NaOH溶液的实验中,如果出现以下操作,会导致配制溶液的浓度偏大的有__(填写字母).
A.称量时用了生锈的砝码 B.未洗涤溶解NaOH的烧杯
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D.容量瓶未干燥即用来配制溶液 E.定容时仰视刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com