
【题目】江苏正在建设世界最大的海上风电场,防腐蚀是海上风电的突出问题,下列说法正确的是

A. 海水的pH一般在8.0~8.5,对风电钢铁支架的腐蚀主要是析氢腐蚀
B. 腐蚀总反应为4Fe+3O2 +2xH2O=2[Fe2O3·xH2O](铁锈)的ΔH <0,ΔS<0
C. 钢部件镀锌前,可用碱液洗去表面的铁锈
D. 热喷涂锌铝合金,可以减缓管道的腐蚀
【答案】BD
【解析】A,海水的pH一般在8.0~8.5,对钢铁支架的腐蚀主要是吸氧腐蚀;B项,腐蚀的总反应为4Fe+3O2+2xH2O=2[Fe2O3·xH2O],该反应为放热反应,ΔS![]() 0;C项,碱液与铁锈不反应;D项,锌铝合金比Fe活泼,锌铝合金为负极,钢铁为正极被保护,减缓管道的腐蚀。
0;C项,碱液与铁锈不反应;D项,锌铝合金比Fe活泼,锌铝合金为负极,钢铁为正极被保护,减缓管道的腐蚀。
A项,海水的pH一般在8.0~8.5,海水呈弱碱性,对钢铁支架的腐蚀主要是吸氧腐蚀,A项错误;B项,钢铁发生吸氧腐蚀的电极反应式为:负极电极反应式为Fe-2e-=Fe2+、正极电极反应式为O2+2H2O+4e-=4OH-,电池总反应为2Fe+O2+2H2O=2Fe(OH)2,接着发生的反应有4Fe(OH)2+O2+2H2O=4Fe(OH)3、2Fe(OH)3=Fe2O3+3H2O,腐蚀的总反应为4Fe+3O2+2xH2O=2[Fe2O3·xH2O],该反应为放热反应,ΔS![]() 0,B项正确;C项,铁锈的主要成分为Fe2O3·xH2O,碱液与铁锈不反应,不能洗去钢部件表面的铁锈,C项错误;D项,锌铝合金比Fe活泼,锌铝合金为负极,钢铁为正极被保护,减缓管道的腐蚀,此保护法称为牺牲阳极的阴极保护法,D项正确;答案选BD。
0,B项正确;C项,铁锈的主要成分为Fe2O3·xH2O,碱液与铁锈不反应,不能洗去钢部件表面的铁锈,C项错误;D项,锌铝合金比Fe活泼,锌铝合金为负极,钢铁为正极被保护,减缓管道的腐蚀,此保护法称为牺牲阳极的阴极保护法,D项正确;答案选BD。


科目:高中化学 来源: 题型:
【题目】下列物质的性质与氢键无关的是( )
A.NH3分子比PH3分子稳定B.通常情况NH3极易溶于水
C.冰的密度小于水的密度D.H2O的沸点比H2S的沸点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推测或结论不合理的是( )
A. X2-和Y+核外电子层结构相同,原子序数:X<Y
B. 气态氢化物的稳定性HCl>HBr,还原性:Cl->Br-
C. 硅、锗都位于金属与非金属的交界处,都可以作半导体材料
D. 铷(37Rb)和锶(38Sr)分别位于第五周期IA和IIA族,碱性:RbOH>Sr(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
CH3COOH | HClO | H2CO3 |
Ka=1.8×10﹣5 | Ka=3.0×10﹣8 | Ka1=4.4×10﹣7 Ka2=4.7×10﹣11 |

A.如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO﹣+CO2+H2O═2HClO+CO32﹣
C.a、b、c三点所示溶液中水的电离程度c>a>b
D.图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.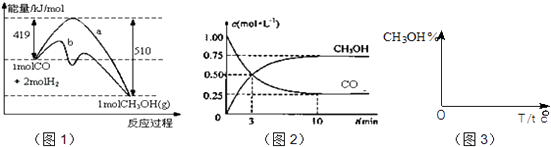
请回答下列问题:
(1)在“图1”中,曲线(填:a或b)表示使用了催化剂;该反应属于反应.
(2)下列说法正确的是 .
A.起始充入的CO为2mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2 , 再次达到平衡时,n(CH3OH)/n(CO)会减小
(3)从反应开始到建成平衡,v(H2)=;该温度下CO(g)+2H2(g)CH3OH(g)的化学平衡常数值为 . 若保持其它条件不变,将反应体系升温,则该反应化学平衡常数(填“增大”、“减小”或“不变”).
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2 , 且P1<P2).
(5)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A、CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
B、CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2O(g);△H=﹣192.9kJ/mol
O2(g)=CO2(g)+2H2O(g);△H=﹣192.9kJ/mol
又知H2O(l)=H2O(g)△H=+44kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.2﹣乙基﹣1,3﹣丁二烯的键线式: ![]()
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等
C.苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.用溴水可鉴别苯、CCl4、苯乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com