
【题目】下列推测或结论不合理的是( )
A. X2-和Y+核外电子层结构相同,原子序数:X<Y
B. 气态氢化物的稳定性HCl>HBr,还原性:Cl->Br-
C. 硅、锗都位于金属与非金属的交界处,都可以作半导体材料
D. 铷(37Rb)和锶(38Sr)分别位于第五周期IA和IIA族,碱性:RbOH>Sr(OH)2
【答案】B
【解析】A项,X2-和Y+核外电子层结构相同,X的核外电子数小于Y的核外电子数,原子序数X![]() Y;B项,非金属性Cl
Y;B项,非金属性Cl![]() Br,气态氢化物的稳定性HCl
Br,气态氢化物的稳定性HCl![]() HBr,还原性Cl-
HBr,还原性Cl-![]() Br-;C项,在金属与非金属的交界处可以找到半导体材料;D项,同周期从左到右元素的金属性逐渐减弱,最高价氧化物对应水化物的碱性依次减弱。
Br-;C项,在金属与非金属的交界处可以找到半导体材料;D项,同周期从左到右元素的金属性逐渐减弱,最高价氧化物对应水化物的碱性依次减弱。
A项,X2-和Y+核外电子层结构相同,X的核外电子数小于Y的核外电子数,原子序数X![]() Y,A项正确;B项,非金属性Cl
Y,A项正确;B项,非金属性Cl![]() Br,气态氢化物的稳定性HCl
Br,气态氢化物的稳定性HCl![]() HBr,还原性Cl-
HBr,还原性Cl-![]() Br-,B项错误;C项,在金属与非金属的交界处可以找到半导体材料,硅、锗都位于金属与非金属的交界处,都可以作半导体材料,C项正确;D项,同周期从左到右元素的金属性逐渐减弱,最高价氧化物对应水化物的碱性依次减弱,金属性Rb
Br-,B项错误;C项,在金属与非金属的交界处可以找到半导体材料,硅、锗都位于金属与非金属的交界处,都可以作半导体材料,C项正确;D项,同周期从左到右元素的金属性逐渐减弱,最高价氧化物对应水化物的碱性依次减弱,金属性Rb![]() Sr,碱性RbOH
Sr,碱性RbOH![]() Sr(OH)2,D项正确;答案选B。
Sr(OH)2,D项正确;答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】我国科学家报道了如图所示的水溶液锂离子电池体系,下列叙述错误的是()
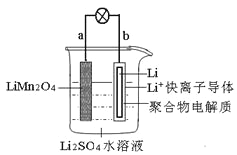
A. 放电时,a极锂的化合价发生变化
B. 电流的方向为a到b
C. a为电池的正极
D. 放电时,溶液中Li+从b向a迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室中某些气体的制备、除杂、收集装置。用此装置能获得干燥纯净气体的是
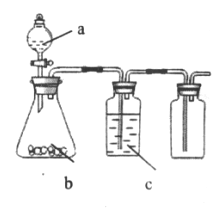
选项 | a | b | c | 气体 |
A | 浓盐酸 | Na2SO3 | 浓硫酸 | SO2 |
B | 稀硝酸 | Cu | 浓硫酸 | NO |
C | 浓盐酸 | MnO2 | 饱和食盐水 | Cl2 |
D | H2O2 | MnO2 | 浓硫酸 | O2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生反应X(g)+2Y(g)![]() 3Z(g)△H=-akJ·mol-1(a>0),下列说法正确的是
3Z(g)△H=-akJ·mol-1(a>0),下列说法正确的是
A. 容器内气体的压强不再发生变化,说明反应达到平衡状态
B. 达到化学平衡状态时,反应放出的总热量可能为akJ
C. 当X、Y、Z的浓度之比为1:2:3时,反应达到化学平衡状态
D. 降低反应温度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个原电池总反应为Zn+Cu2+=Zn2++Cu,该电池电极材料及电解质溶液可能是 ( )
选项 | 正极 | 负极 | 电解质溶液 |
A | Zn | Cu | CuCl2 |
B | Zn | Cu | H2SO4 |
C | Cu | Zn | CuSO4 |
D | Zn | Ag | CuSO4 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. H2O的沸点比H2S高,所以H2O比H2S更稳定
B. 干冰和石英晶体中的化学键类型相同,熔化时需克服微粒间的作用力类型也相同
C. N2和CCl4中,每个原子的最外层都具有8电子稳定结构
D. NaHCO3受热分解的过程中,只有离子键被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】江苏正在建设世界最大的海上风电场,防腐蚀是海上风电的突出问题,下列说法正确的是

A. 海水的pH一般在8.0~8.5,对风电钢铁支架的腐蚀主要是析氢腐蚀
B. 腐蚀总反应为4Fe+3O2 +2xH2O=2[Fe2O3·xH2O](铁锈)的ΔH <0,ΔS<0
C. 钢部件镀锌前,可用碱液洗去表面的铁锈
D. 热喷涂锌铝合金,可以减缓管道的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图提供的信息,下列所得结论不正确的是( )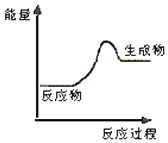
A.该反应可能为吸热反应
B.该反应一定有能量转化成了生成物的化学能
C.反应物比生成物稳定
D.生成物的总能量高于反应物的总能量,反应不需要加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸乙酯,如图1所示实验装置: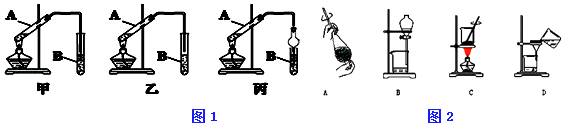
请回答下列问题:
(1)能完成本实验的装置是(从甲、乙、丙中选填)
(2)试管B中装入的液体为 . 试管B中发生反应的化学方程式为 .
(3)制取乙酸乙酯时加入试剂顺序为 , 发生反应的化学方程式为 .
(4)从制备乙酸乙酯所得的混合物中分离、提纯乙酸乙酯时,需要经过多步操作,下列图2示的操作中,肯定需要的化学操作是(选填答案编号).
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器.使用分液漏斗前必须;某同学在进行分液操作时,若发现液体流不下来,应采取的措施是 .
(6)用30g乙酸和40g乙醇反应,可以得到37.4g乙酸乙酯,则该实验的产率(产率指的是某种生成物的实际产量与理论产量的比值)是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com