
一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是
A. 9.2g B.10.6g C.6.2g D.4.6g
科目:高中化学 来源: 题型:
工业上为了测定辉铜矿(主要成分是Cu2S)中Cu2S的质量分数,设计了如图装置。实验时按如下步骤操作:
A. 连接全部仪器,使其成为如图装置,并检查装置的气密性。
B. 称取研细的辉铜矿样品1.000g。
C. 将称量好的样品小心地放入硬质玻璃管中。
D. 以每分钟1L的速率鼓入空气。
E.将硬质玻璃管中的辉铜矿样品加热到一定温度,发生反应为:Cu2S+O2=SO2 +2Cu。
F. 移取25.00ml含SO2的水溶液于250ml锥形瓶中,用0.0100mol/L KMnO4标准溶液滴定至终点。按上述操作方法重复滴定2—3次。

试回答下列问题:
(1)装置①的作用是_________________;装置②的作用是____________________。
(2)假定辉铜矿中的硫全部转化为SO2,并且全部被水吸收,则操作F中所发生反应的化学方程式为 ,当产生______________________________ _的现象时可判断滴定已经达到终点。
(3)若操作F的滴定结果如下表所示,则辉铜矿样品中Cu2S的质量分数是_________。
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.04 | 21.03 |
| 2 | 25.00 | 1.98 | 21.99 |
| 3 | 25.00 | 3.20 | 21.24 |
(4)本方案设计中由一个明显的缺陷影响了测定结果(不属于操作失误),你认为是
(写一种既可)。
(5)已知在常温下FeS 的 Ksp= 6 . 25 × 10 -18, H2S 饱和溶液中 c (H+)与 c (S2-)之间存在如下关系: c2 (H+) ·(S2-) = 1 . 0×10-22 。在该温度下,将适量 FeS 投入硫化氢饱和溶液中,欲使溶液中(Fe2+)为 lmol/L,应调节溶液的c(H十)为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中实验操作能达到实验目的的是 ( )
| 选项 | 实 验 操 作 | 实 验 目 的 |
| A | 向过量的苯酚溶液中加入少量的溴水 | 观察生成的白色沉淀三溴苯酚 |
| B | 向甲酸钠溶液中加新制的Cu(OH)2悬浊液并加热 | 确定甲酸钠中含有醛基 |
| C | 向酒精和醋酸的混合液中加入金属钠 | 确定酒精中混有醋酸 |
| D | 将溴乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的溴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质:①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A.①④⑥ B. ②③④ C.②③⑤ D. ①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
有Mg、Al、Fe、Cu四种金属,若两两混合,取混合物26g与足量稀硫酸反应,产生标准状况下H2 11.2L。此混合物的可能组成方式最多有
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)有一瓶存放时间较长的硫酸亚铁,外观上并无明显变化,但某学生怀疑其有部分因氧化而变质,请你设计1个检验硫酸亚铁是否变质的实验方案: 。如果有变质,当配制硫酸亚铁溶液时,应如何除去变质的杂质? 。(2)FeCl3溶液棕黄色,对此溶液,分别做如下实验,请填表:
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量铁粉 | ||
| ② | 加入少量Na2O2粉末 | ||
| ③ | 加入少量AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
中国气象局的数据显示,2013年全国平均雾霾天数为52年来之最。形成雾霾的主要成份为:生产生活中排放的废气、汽车尾气及扬尘等。
(1)用CH4可以消除汽车尾气中氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l) △H=-955 kJ·mol-1
2NO2(g)=N2O4(g) △H=-56.9 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式 。
(2)已知:CO(g)+H2O(g)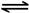 CO2(g)+H2(g) △H=-41kJ·mol-1,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0molH2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则t min内用H2表示的平均反应速率为 ,由此可知在该温度下反应CO2(g)+H2(g)
CO2(g)+H2(g) △H=-41kJ·mol-1,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0molH2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则t min内用H2表示的平均反应速率为 ,由此可知在该温度下反应CO2(g)+H2(g)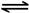 CO(g)+H2O(g)的化学平衡常数为 。相同条件下,向同一密闭容器中充入1.0molCO2和1.0molH2反应达到平衡后,吸收的热量为 kJ。
CO(g)+H2O(g)的化学平衡常数为 。相同条件下,向同一密闭容器中充入1.0molCO2和1.0molH2反应达到平衡后,吸收的热量为 kJ。
(3)碱式硫酸铝法烟气脱硫工艺主要有以下三步
①向Al2(SO4)3溶液中投入粉末状石灰石,生成碱式硫酸铝[Al2(SO4)3·Al2O3]溶液。
②碱式硫酸铝吸收SO2,Al2(SO4)3·Al2O3+3SO2=Al2(SO4)3·Al2(SO3)3,请写出Al2(SO4)3·Al2O3与过量烧碱溶液反应的化学方程式 。
③将Al2(SO4)3·Al2 (SO3)3氧化成Al2(SO4)3,可选用氧化剂为 (填代号)
a. 浓硫酸 b. KMnO4溶液 c. 5%的H2O2溶液 d. 空气
该步反应的目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色电源“二甲醚-氧气燃料电池”的工作原理如下图,所示下列说法正确的是
A.氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O==4OH-
B.电池在放电过程中,电极X周围溶液的pH增大
C.二甲醚应从b处加入,电极X上发生的反应为(CH3)2O -12e-+3H2O=2CO2+12H+
D.当该电池向外电路提供2mol电子时消耗O2约为22.4L
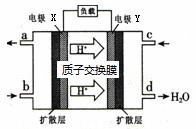
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com