
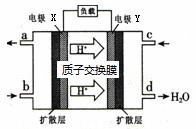
绿色电源“二甲醚-氧气燃料电池”的工作原理如下图,所示下列说法正确的是
A.氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O==4OH-
B.电池在放电过程中,电极X周围溶液的pH增大
C.二甲醚应从b处加入,电极X上发生的反应为(CH3)2O -12e-+3H2O=2CO2+12H+
D.当该电池向外电路提供2mol电子时消耗O2约为22.4L
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是
A. 9.2g B.10.6g C.6.2g D.4.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断不正确的是 ( )
①都是主族元素,原子的最外层电子数都大于3;②单质在反应中都只能作氧化剂;③对应的含氧酸都是强酸;④氢化物常温下都是气态,所以又叫气态氢化物;⑤氧化物与水反应都不会再生成气体
A.全部 B.只有① C.只有①②③ D.只有①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D.第三周期元素的离子半径从左到右逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是周期表的一部分,A、B、C、D、E 5种元素的原子核外共含有80个电子。
|
A C
(2)A、B、C的最高价含氧酸的酸性由强到弱的顺序是(用化学式表示) 。
(3)A的最高价氧化物对应的水化物体现 (填“酸性 ”、“碱性”、“两性”),体现酸性的离子方程式表示为:
(4)E为 (填“金属”、“非金属”),其单质可能为 (填“导体”、“非导体”、“半导体”),推断理由是
查看答案和解析>>
科目:高中化学 来源: 题型:
研究化肥的合成、废水的处理等有现实的重要意义。
Ⅰ.尿素是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g) H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
试回答下列问题:
(1)下列措施中有利于提高尿素的产率的是___________。
A.采用高温 B.采用高压 C.寻找更高效的催化剂
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l) △H1
H2NCOONH4(氨基甲酸铵) (l) △H1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
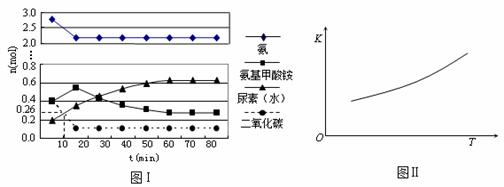 |
① 已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
② 反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)= 。
③ 第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2 0
(填“>”“<”或“=”)
Ⅱ.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42 g/L | 1.6 g·L-1 |
| 排放标准 | pH 6~9 | 0.5 mg·L-1 |
表1.几种砷酸盐的Ksp 表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
(3)若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol·L-1,
c(AsO43-)最大是 mol·L-1。
(4)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式 。
(5)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
① 将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为 ;
② Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列行为中符合安全要求的是( )
A 进入煤矿井时,用火把照明 B 节日期间,在开阔的广场燃放烟花爆竹
C 用点燃的火柴在液化气钢瓶口检验是否漏气 D 实验时,将水倒入浓硫酸配制稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
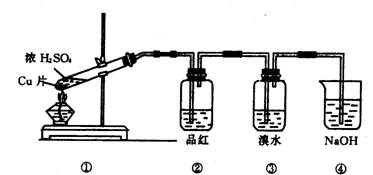
根据下图所示的实验装置,回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式
(2)证明SO2具有漂白性的现象是 ,再加热该溶液,现象是 .
(3)装置③中的现象是 ,证明SO2具有 .
(4)装置④的作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com