
 HClO +OH- ��2�֣� ��3��c(ClO-)��c(Ca2+)��c(OH-)��c(H+)��1�֣�
HClO +OH- ��2�֣� ��3��c(ClO-)��c(Ca2+)��c(OH-)��c(H+)��1�֣� HClO +OH- ��
HClO +OH- ��

 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʯ�� | B�������� | C���������� | D���Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ƿ�����������ȼ�գ�������ɫ���� |
| B�����ȵ�ͭ˿������������ȼ�գ�������ɫ���� |
| C�����������������������а���ȼ�գ�������ɫ���� |
| D�����������ڸ����Ʒ����ֽ����ֽ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
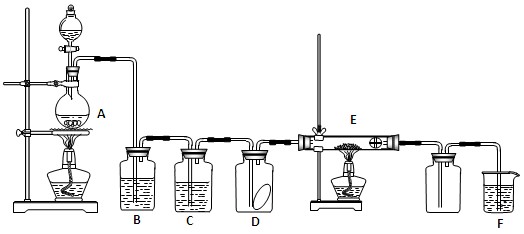
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������ʸ�����������Ӧ | B��HClO4���Ա�H2SO4ǿ |
| C��������ǿ�ᣬ������������ | D������ʱ���Ȼ���������ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��HClO��Ư���� | B��HClO�IJ��ȶ��� |
| C��HClO�������� | D��H2CO3������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaCl��I2��Cl2 | B��NaCl��I2 | C��NaCl��NaBr | D��NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��BrCl��NaOH��Һ��Ӧ����NaCl��NaBrO������ |
| B��BrCl���н�ǿ�������� |
| C����ʹ��ʪ�ĵ��۵⻯����ֽ���� |
| D��BrCl��ˮ��Ӧ�У�BrCl�������������ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com