
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )

A. 在0-a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
【答案】C
【解析】A、向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸发生的反应依次为H++OH-=H2O、CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑,第三步才开始产生气体,故0-a范围内,发生了前两步反应,A错误;B、ab段立即产生气体,则反应为: HCO3-+H+=H2O+CO2↑,故B错误;C、生成CO2 0.01mol,根据方程式HCO3-+H+=H2O+CO2↑可知,消耗盐酸的物质的量是0.01mol,消耗盐酸的体积为0.1L,所以a=0.3,故C正确;D、生成0.01mol CO2,则Na2CO3为0.01mol,Na2CO3共消耗盐酸0.02mol,从图上可知整个过程共消耗0.04molHCl,所以与NaOH反应的盐酸是0.04mol-0.02mol=0.02mol,则NaOH为0.02mol,因此原混合溶液中NaOH与Na2CO3的物质的量之比为2:1,故D错误。选C。


科目:高中化学 来源: 题型:
【题目】下图是关于反应A2(g)+3B2(g) ![]() 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是

A. 升高温度,同时加压
B. 降低温度,同时减压
C. 增大反应物浓度,同时使用催化剂
D. 增大反应物浓度,同时减小生成物浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微粒用AZXn+表示,下列关于该微粒的叙述正确的是( )
A. 所含质子数= A-n B. 所含电子数=Z+n
C. 质量数=Z+A D. 所含中子数=A-Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B都为短周期元素,且甲、乙、丙常温下都为气体(如图所示)。2 mol甲分子反应生成1 mol 丙和3 mol乙,下列对此判断不正确的是( )

A. 1个乙分子中含有2个A原子
B. 甲的摩尔质量为17 g·mol-1
C. 同温同压下,生成丙和乙的体积比为1∶3
D. 标准状况下,11.2 L甲溶于500 mL水中,所得溶液中甲的物质的量浓度为1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素及其化合物的知识是高中化学重要的组成部分,是考查化学基本概念和理论、化学计算、化学实验知识的载体。
(1)元素周期表1-20号元素中,某两种元素的原子序数相差3,周期数相差1。
①这样的两种元素的组合有________种。
②若这样的两种元素形成的化合物中原子数之比为1∶1。
写出其中一种化合物的名称:_______________________;
(2)A是自然界存在最广泛的ⅡA族元素,常以化合物F存在.从单质A起始发生的一系列化学反应可由下图表示:
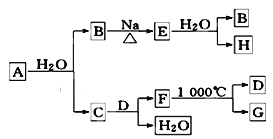
请回答下列问题:
①F的化学式为________,D的电子式为________________。
②E与水反应的化学方程式为___________________________________________;
③实际生产中,可由F为原料制备单质A,写出制备过程的化学方程式(不需考虑综合经济效益)_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1:2,则加入铝粉的质量为( )
A. 1.8 g B. 2.7 g C. 3.6 g D. 5.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,A与B反应生成C,其反应速率的关系为:vA=3vB、2vA=3vC,则该反应可表示为
A. 2A+ 6B =3C B. A+ 3B =2C C. 3A+ B =2C D. 2 A+ 3B =2C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com