
【题目】下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是( )

A. 向盐酸和氯化钙的混合溶液中加入碳酸钠 B. 向氢氧化钠溶液中加水
C. 双氧水分解 D. 向饱和氯化钠溶液中加水稀释
【答案】D
【解析】
A、向盐酸和氯化钙的混合溶液中加入碳酸钠,碳酸钠会先与盐酸反应,再和氯化钙反应产生沉淀;B、氢氧化钠中加水溶液碱性会减弱;C、过氧化氢溶液制氧气时加入二氧化锰不会增加氧气的产量,只会加快反应的速度;D、饱和氯化钠溶液加水时溶质的质量保持不变,会使溶质质量分数减小。
A、向盐酸和氯化钙的混合溶液中加入碳酸钠,碳酸钠会先与盐酸反应,不会生成沉淀,直至盐酸完全反应,再和氯化钙反应产生沉淀,故A正确;B、氢氧化钠中加水稀释后溶液碱性会减弱,PH减小但不会小于7,故B正确;C、过氧化氢溶液制氧气加入二氧化锰不会增加氧气的产量,只会加快反应的速度,故C正确;D、饱和氯化钠溶液加水稀释,溶质质量分数减小,但溶质的质量不会改变,与图象不相符,故D错误。故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硼酸(H2BO3)可以通过电解NaB(OH)4溶液的方法制备,工作原理如图所示。下列有关表述错误的是( )
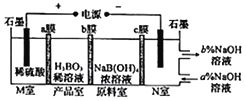
A. M室的电极反应式为2H2O-4e-=O2↑+4H+
B. N室中,进口和出口的溶液浓度大小关系为a%<b%
C. b膜为阴离子交换膜,产品室发生反应为H++[B(OH)4]-=H3BO3+H2O
D. 理论上每生成1molH3BO3,阴极室可生成5.6L气体(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某羧酸酯的分子式为C18H26O5,1mol该酯完全水解得到1mol羧酸和2mol乙醇,该羧酸的分子式为
A. C16H22O5 B. C14H16O4 C. C16H20O4 D. C14H18O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩拜单车利用车篮处的太阳能电池板向智能锁中的锂离子电池充电,电池反应原理为LiCoO2 +6C![]() li1-xCoO2 +lixC6,结构如图所示。下列说法正确的是
li1-xCoO2 +lixC6,结构如图所示。下列说法正确的是
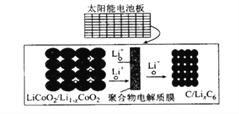
A. 放电时,正极质量增加
B. 充电时,锂离子由右向左移动
C. 该钾离了电池工作时,涉及到的能量形式有3 种
D. 充电时、阳极的电极反应式为Li1-xCoO2+xLi++xe-= LiCoO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。
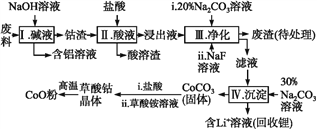
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表。
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是__________。
(2)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:______。
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过______;废渣中的主要成分除了LiF外,还有______。
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是______。
(5)在空气中加热5.49 g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~920 | 2.25 |
①加热到210 ℃时,固体质量减轻的原因是__________。
②经测定,加热到210~290 ℃过程中的生成物只有CO2和钴的氧化物span>,此过程发生反应的化学方程式为___________。[已知M(CoC2O4·2H2O)=183 g·mol-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭绝热容器中发生反应:SO2(g)+NO2(g) ![]() SO3(g)+NO(g) △H<0下列有关说法不正确的是 ( )
SO3(g)+NO(g) △H<0下列有关说法不正确的是 ( )
A. 增大SO2的浓度,平衡正向移动
B. 使用催化剂,正反应速率和逆反应速率同时增大
C. 反应达到平衡时,扩大容器体积,平衡逆向移动
D. 反应达到平衡时,降低温度,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由含铜废料制铜的一种方案是:
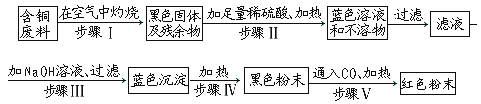
(1)写出下列步骤中的化学方程式:步骤Ⅲ:_________.步骤V:_________.
(2)步骤Ⅱ后形成的蓝色溶液中的溶质是_________.
(3)上述方案中可能造成空气污染的步骤是_________.
(4)若含铜废料的质量为a千克,黑色粉末的质量b千克,则该含铜废料中的含铜量为:___________(用含a,b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )

选项 物质 | a | b | c |
A | Al | AlCl3 | Al(OH)3 |
B | HNO3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | S | SO2 | H2SO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理的利用吸收工业产生的废气CO2、NO2、SO2 等可以减少污染,变废为宝。
(1)用CO2可以生产燃料甲醇。
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=﹣akJmol﹣1;
2H2(g)+O2(g)═2H2O(l)△H=﹣b kJmol﹣1;
则表示CH3OH(g)燃烧的热化学方程式为:
_______________________________________________________。
(2)光气(COCl2)是一种重要化工原料,常用于聚酯类材料的生产,工业上通过Cl2(g)+CO(g)COCl2(g)△H < 0制备。图1为实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:

①0~6min内,反应的平均速率v(Cl2)=_______;
②该反应第一次达平衡时的平衡常数为__________,10min改变的条件是______。
(3)利用氨水可以将SO2和NO2吸收,原理如图2所示:NO2被吸收的离子方程式是___________________________________。

(4)以甲醇燃料电池为电源,粗硅为原料,熔融盐电解法制取硅烷原理如图3,判断A为电源的___极,电解时阳极的电极反应式为_____。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com