
五颜六色的颜色变化增添了化学的魅力,下列有关反应的颜色叙述正确的是 ( )
①新制氯水久置后→浅黄绿色消失 ②淀粉溶液遇单质碘→蓝色 ③溴化银见光分解→银白色 ④Na2CO3溶液中滴加酚酞→红色 ⑤鸡蛋白溶液遇浓硝酸→黄色 ⑥碘化银的悬浊液中加入硫化钠晶体,振荡后变黑
A.①②③④⑤ B.②③④⑤⑥
C.①②④⑤⑥ D.①③④⑤⑥
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
下列离子方程式不正确的是 ( )
A.石英与烧碱反应:SiO2+2OH-===SiO +H2O
+H2O
B.硅与烧碱反应:Si+2OH-===SiO +H2↑
+H2↑
C.硅酸钠溶液中通入少量CO2:SiO +CO2+H2O===CO
+CO2+H2O===CO +H2SiO3↓
+H2SiO3↓
D.往水玻璃中加入盐酸:2H++SiO ===H2SiO3↓
===H2SiO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO 、NO
、NO 、SO
、SO 、SiO
、SiO 。
。
现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化。
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅲ.向Ⅱ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅳ.向Ⅱ中所得的溶液中加入过量浓氨水,仅有红褐色沉淀生成。过滤,在所得滤液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
请回答下列问题:
(1)该废水中一定含有的离子是___________________________。
(2)实验Ⅱ中加入少量盐酸生成无色气体的离子方程式是_________________________________________________________。
(3)过滤除去Ⅳ中的蓝色沉淀,调整滤液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为14,其离子方程式为Al+NO +OH-―→AlO
+OH-―→AlO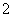 +NH3+N2+H2O(未配平)。还原产物是________。若除去0.2 mol NO
+NH3+N2+H2O(未配平)。还原产物是________。若除去0.2 mol NO ,要消耗铝________g。
,要消耗铝________g。
(4)工业废水中常含有不同类型的污染物,可采用不同的方法处理。下列处理措施和方法中正确的是________。
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 碱性的废水 | 用CO2中和 | 化学法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 废酸 | 加生石灰中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式IBr+H2O===HBr+HIO,下列有关IBr的叙述中,不正确的是 ( )
A.IBr是双原子分子
B.在很多反应中,IBr是强氧化剂
C.和NaOH溶液反应生成NaBr和NaIO
D.和水反应时,既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)(3))二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。某次除杂操作时,往粗盐水中先加入过量的________________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发
等杂质。某次除杂操作时,往粗盐水中先加入过量的________________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发
现滤液中仍含有一定量的SO ,其原因是________________________________[已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaCO3)=5.1×10-9]。
,其原因是________________________________[已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaCO3)=5.1×10-9]。
②该法工艺原理示意图如下。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。工艺中可以利用的单质有____________(填化学式),发生器中生成ClO2的化学方程式为_____________________________________________________
________________________________。

(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理 含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的______倍。
含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
取体积相同的KI、Na2SO3、FeBr2溶液,分别通入足量氯气,当恰好完全反应时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2溶液的物质的量浓度之比为( )
A.2∶1∶2 B.2∶1∶3
C.6∶3∶2 D.3∶7∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物W( )常用于合成维生素类药物。下列与W相关说法正确的是
)常用于合成维生素类药物。下列与W相关说法正确的是
A.分子式为C6H9O3
B.分子中含有2种官能团
C.分子中含有6种不同化学环境的氢原子
D.水溶液中lmolW可与3molNaOH完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 右图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是( )
右图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是( )
A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH
D.电解一段时间后加适量盐酸可以恢复到电解前的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①离子化合物含离子键,也可能含极性键或非极性键 ②H2SO3的酸性>H2CO3的酸性,所以非金属性S>C ③含金属元素的化合物不一定是离子化合物 ④由非金属元素组成的化合物一定是共价化合物 ⑤熔融状态能导电的化合物是离子化合物 ⑥由分子组成的物质中一定存在共价键
A.①③⑤⑥ B.②④⑥ C.①②③⑤ D.①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com