
25℃和101kPa时,乙烯、乙炔和丙炔组成的混合烃20mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了35mL,原混合烃中乙炔的体积分数为 ( )
A. 75% B. 12.5% C. 25% D. 50%
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
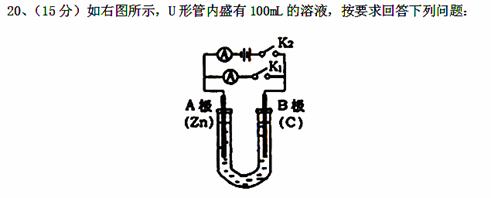
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为 极, A极的电极反应式为 。若所盛溶液为KCl溶液:则B极的电极反应式为
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:
①A电极附近可观察到的现象是 ,Na+移向 极(填A、B)
②B电极上的电极反应式为 ,
总反应化学方程式是 。
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的 。[ pH=-lgc(H+) ]
查看答案和解析>>
科目:高中化学 来源: 题型:
我们知道海带中含有碘元素,经常食用海带可以防治甲状腺肿大,所以工业上常用海带为原料提取碘单质。查有关资料可知碘单质有升华现象。下面是某校化学探究小组设计的从海带中提取单质碘的实验,请你完成下列实验。
(1)将干燥洁净的海带用酒精湿润后在__________(填一种仪器名称)中灼烧成灰烬。
(2)将海带灰烬冷却至室温,转移到烧杯中,加蒸馏水后,搅拌、煮沸、冷却、__________(填一种操作名称)。
(3)在滤液中滴入几滴稀硫酸,再加入一定量的过氧化氢溶液,此时发生反应的离子方程式为:__________________________________。
(4)把(3)中所得到的溶液注入分液漏斗中,然后再加入四氯化碳,振荡、静置,可以观察到四氯化碳层呈________色。经分液得到碘的四氯化碳溶液,在这一实验过程中,四氯化碳起____________作用。
(5)用试管取碘的四氯化碳溶液用水浴加热,待四氯化碳挥发完即可得到固体碘单质。为什么不用酒精灯直接加热蒸发四氯化碳:_____________________________。
(6)证明得到的固体是碘单质的化学方法是_____________________________________
__________________________________ ______________________________________。
______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯水中含有多种成分,因而具有多种
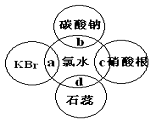 性质,根据氯水分别与如图四种物质发生的反应
性质,根据氯水分别与如图四种物质发生的反应
填空(a、b、c、d重合部分代表物质间反应,且氯水
足量)。
能证明氯水具有漂白性的是__________(填“a”、“b”、“c”或“d”)。
(1)C过程中的现象是_______________________,b过程中的离子方程式为
_____________________________________(提示:酸性H2CO3 > HClO > HCO3-)。
(2)a过程中的化学方程式为________________________________________。
(4)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO—与ClO3—的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
橡胶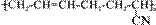
 具有优良的耐油、耐高温性能,合成该橡胶的原料是( )
具有优良的耐油、耐高温性能,合成该橡胶的原料是( )
① CH2=CH-CH=CH2 ②CH3-C C-CH3 ③CH2=CH-CN
C-CH3 ③CH2=CH-CN
④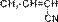 ⑤ CH3-CH=CH2 ⑥ CH3-CH=CH-CH3
⑤ CH3-CH=CH2 ⑥ CH3-CH=CH-CH3
A.③ ⑥ B .② ③ C. ① ③ D. ④ ⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G均为有机化合物。
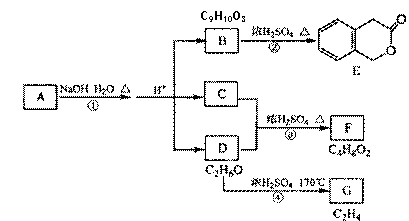 |
根据上图回答问题:
(1)A的分子式是 ,B 的结构简式是
(2)反应③的化学方程式是 。
(3)写出反应①至④中属于消去反应的化学方程式 。
(4)符合下列3个条件的B的同分异构体的所有的结构简式
(i). 可发生银镜反应
(ii) 核磁共振氢谱有5种峰
(iii)与FeCl3溶液发生显色反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法正确的是( )
A.1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子
B.1 mol Al分别放入足量的冷的浓HNO3、稀HNO3中,反应后转移的电子均为3NA
C.各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA
D.24 g镁与足量的盐酸或NaOH溶液反应转移的电子数目均为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
为了预防碘缺乏病,有关部门规定食盐中的碘含量(以I计)应在20~50 mg/kg。制备KIO3的方法如下:
方法1:6I2+11KClO3+3H2O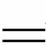 6KH(IO3)2+5KCl+3Cl2↑
6KH(IO3)2+5KCl+3Cl2↑
KH(IO3)2+KOH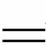 2KIO3+H2O
2KIO3+H2O
方法2:碱性条件下,KI+3H2O KIO3+3H2↑
KIO3+3H2↑
方法3:I2 HIO3
HIO3 KIO3
KIO3
(1)与方法3相比方法1的不足是________________________________________________________________________,
方法2的不足是________________________________________________________________________。
(2)方法2选用的电极是惰性电极,则其阳极反应式是________________________________________________________________________。
(3)方法3反应温度控制在70 ℃左右,不采用更高温度的主要原因是________________________________________________________________________。
(4)制备纯净KIO3的实验步骤中,最后需将所得晶体最好使用____________________洗涤2~3次,干燥后得产品。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com