
【题目】下列变化或数据与氢键无关的是( )
A. 水的沸点比硫化氢的沸点高
B. 氨分子与水分子形成一水合氨
C. 乙醇能跟水以任意比混溶
D. SbH3的沸点比PH3高
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题:
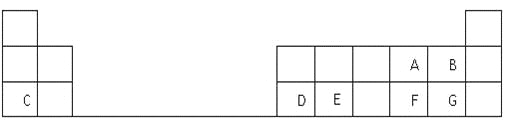
(1)G在元素周期表中的位置是 。
(2)A、B、C三种元素的简单离子半径由大到小的顺序为 (用离子符号表示)。
(3)写出C和F两种元素形成的化合物的电子式 ,
(4)元素E是构成地壳的主要元素之一,其氧化物是制光导纤维的基本原料,该氧化物中含有的化学键是 键(填“离子”或“共价”),属于 晶体(填晶体类型),写出该氧化物与C元素最高价氧化物水化物反应的离子方程式 。
(5)C离子的氧化性比D离子的氧化性 ,(填“强”或“弱”),其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列晶体中含有非极性共价键的离子晶体是( )
①硅晶体 ②H2O2 ③CaC2 ④NH4Cl ⑤Na2O2 ⑥苯酚
A.①②④⑥ B.①③ C.②④⑤⑥ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论错误的是( )
A.氯化铝是电解质
B.固体氯化铝是分子晶体
C.可用电解熔融氯化铝的办法制取金属铝
D.氯化铝为非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NaCl等为原料制备KClO4的过程如下:
①在无隔膜、微酸性条件下,发生反应:NaCl+H2O—NaClO3+H2↑(未配平)
②在NaClO3溶液中加入KCl发生复分解反应,降温结晶,得KClO3。
③一定条件下反应:4KClO3=3KClO4+KCl,将产物分离得到KClO4。

(1)电解时,产生质量为2.13g NaClO3,同时得到H2的体积为________L(标准状况)。
(2)向NaClO3溶液中加入KCl能得到KClO3的原因是______________。
(3)该过程制得的KClO4样品中含少量KCl杂质,为测定产品纯度进行如下实验:
准确称取5.689g样品溶于水中,配成250mL溶液,从中取出25.00mL于锥形瓶中,加入适量葡萄糖,加热使ClO4-全部转化为Cl-(反应为:3 KClO4 +C6H12O6 ═ 6 H2O + 6 CO2↑ + 3 KCl),加入少量K2CrO4溶液作指示剂,用0.20mol/L AgNO3溶液进行滴定至终点,消耗AgNO3溶液体积21.00mL。滴定达到终点时,产生砖红色Ag2CrO4沉淀。
①已知: Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若c(CrO42-)=1.1×10-4mol/L,则此时c(Cl-)=__________mol/L。
②计算KClO4样品的纯度(请写出计算过程。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。经测定:1000g某海带样品中含有6.35g碘离子。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
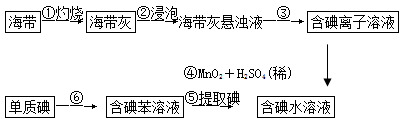
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,将标号字母填写在空白处)。
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是
(3)步骤④反应的离子方程式是_
(4)步骤⑤中,某学生选择用苯来提取碘的理由是
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
(6)从含碘单质的有机溶液中分离出单质碘和回收有机溶剂,应选择的实验装置是
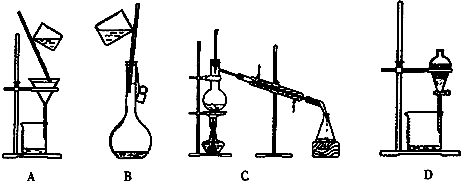
(7)若将l000g上述海带中的碘离子全部氧化,至少需要通入标准状况下的氯气的体积为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
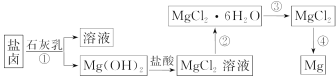
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是___ __ __ __ __ ___。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有__ ___ _溶液(填写化学式)的烧杯中,充分搅拌后经__ _ __ _ __、__ _ __ __ __(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:

其中装置A的作用是___ ___ __ _ __ __ ___ __ __。
(4)写出过程④中发生反应的化学方程式___ __ __ __ __ ___。
(5)金属Mg在CO2中完全燃烧生成MgO和C,下列说法正确的是___ ___。
A.碳单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒半径:r(Mg2+) > r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮及其化合物的性质具有极为重要的意义。
(1) NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_____________________________
(2)在含Cu+离子的酶的活化中,亚硝酸根 (NO2-)离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式 。
(3)将38.4 g铜与150mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L,请回答:
① NO2的体积为____________L。
②若铜与硝酸刚好反应完全,则原硝酸溶液的浓度为____________molL-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com