
【题目】(1)盐酸中加入少量K2FeO4固体,产生黄绿色气体。该反应的化学方程式是___。
(2)用NaClO-NaOH溶液氧化AgNO3,制得高纯度的纳米级Ag2O2。写出该反应的离子方程式:___。
(3)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:___。
(4)Cl2与热的NaOH溶液反应生成NaClO3,该反应的离子方程式为___。
(5)在酸性条件下,NaHSO3使Cr2O72-还原成为Cr3+,写出该反应的离子方程式:___。
【答案】2K2FeO4+16HCl=4KCl+2FeCl3+3Cl2↑+8H2O 2Ag++ClO+2OH=Ag2O2↓+Cl+H2O 2Mg(OH)2+2SO2+O2=2MgSO4+2H2O 3Cl2+6OH![]() ClO3+5Cl+3H2O 3HSO3+Cr2O72+5H+=2Cr3++3SO42+4H2O
ClO3+5Cl+3H2O 3HSO3+Cr2O72+5H+=2Cr3++3SO42+4H2O
【解析】
(1)产生黄绿色气体,可知此反应发生氧化还原反应,根据电子守恒和原子守恒书写方程式;
(2)用NaClO-NaOH溶液氧化AgNO3,制得高纯度的纳米级Ag2O2,同时生成氯化钠和水,结合原则守恒和电荷守恒配平书写离子方程式;
(3)向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,应生成硫酸镁,则反应物还应有氧气,据此分析书写方程式;
(4) Cl2与热的NaOH溶液反应生成NaCl、NaClO3和水;
(5)在酸性条件下,NaHSO3使Cr2O72还原成为Cr3+,NaHSO3被氧化为硫酸钠,结合得失电子守恒和原子守恒分析。
(1)盐酸中加入少量K2FeO4固体,产生黄绿色气体。可知此反应发生氧化还原反应,还原产物应为FeCl3,根据电子守恒和原子守恒可知发生反应的化学方程式为2K2FeO4+16HCl=4KCl+2FeCl3+3Cl2↑+8H2O;
(2)用NaClONaOH溶液氧化AgNO3,制得高纯度的纳米级Ag2O2,同时还会生成NaCl和水,氧元素从2价被氧化成Ag2O2中的1价,化合价至少升高2价;NaClO中Cl元素从+1价被还原为1价的Cl,然后结合原则守恒和电荷守恒配平,该反应的离子方程式为:2Ag++ClO+2OH=Ag2O2↓+Cl+H2O;
(3)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,应生成硫酸镁,则反应物还应有氧气,反应的化学方程式为2Mg(OH)2+2SO2+O2=2MgSO4+2H2O;
(4) Cl2与热的NaOH溶液反应生成NaCl、NaClO3和水,该反应的离子方程式为:3Cl2+6OH![]() ClO3+5Cl+3H2O;
ClO3+5Cl+3H2O;
(5)在酸性条件下,NaHSO3使Cr2O72还原成为Cr3+,NaHSO3被氧化为硫酸钠,反应的离子方程式为:3HSO3+Cr2O72+5H+=2Cr3++3SO42+4H2O。


科目:高中化学 来源: 题型:
【题目】中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银精矿(其化学成分有:Ag、Zn、Cu、Pb、S及SiO2等)中提取银、铜和铅,工艺流程如图所示。

(1)步骤①当盐酸的浓度和KClO3的量一定时,写出两点可提高“浸取”速率的措施______;从Cu和Pb混合物中提取Cu的试剂为______(填名称)。
(2)步骤③反应的化学方程式为______。
(3)步骤④分离出的滤渣中主要含有两种杂质,为了回收滤渣中的非金属单质,某实验小组向滤渣中加入试剂______(填化学式),充分溶解后过滤,然后将滤液进行______(填操作名称),得到该固体非金属单质。
(4)步骤⑤反应中氧化剂和还原剂的物质的量之比为______。
(5)排放后的废水中含有NO3-,任意排放会造成水体污染,科技人员在碱性条件下用Al粉将NO3-还原成无污染气体排放,该方法的缺点是处理后的水中生成了AlO2-,依然对人类健康有害。该反应的离子方程式为:______。25℃时,欲将上述处理过的水中的c(AlO2-)降到1.0×10-7mol/L,此时水中c(Al3+)=______molL-1.(已知,25℃,Ksp(Al(OH)3]=1.3×10-33,Al(OH)3(s)H++AlO2-+H2O,Ka=1.0×10-13)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氨酯类高分子材料PU用途广泛,其合成反应为n![]() +(n+1)HO(CH2)4OH
+(n+1)HO(CH2)4OH![]()
![]() 。下列说法错误的是( )
。下列说法错误的是( )
A.![]() 的沸点高于
的沸点高于![]()
B.高分子材料PU在强酸、强碱条件下能稳定存在
C.合成PU的两种单体的核磁共振氢谱中均有3组吸收峰
D.以1,![]() 丁二烯为原料,可合成
丁二烯为原料,可合成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.1 mol Cl2参加反应转移电子数一定为2NA
B.在反应KIO3 + 6HI = KI + 3I2 +3H2O中,每生成3 mol I2转移的电子数为6NA
C.根据反应中HNO3(稀)![]() NO,而HNO3(浓)
NO,而HNO3(浓)![]() NO2可知,氧化性:HNO3(稀) > HNO3(浓)
NO2可知,氧化性:HNO3(稀) > HNO3(浓)
D.含有大量NO3-的溶液中,不能同时大量存在H+、Fe2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些共价键的键长数据如下表所示。试根据下表回答问题。
共价键 |
|
|
|
|
|
|
|
|
键长 | 0.154 | 0.134 | 0.121 | 0.143 | 0.123 | 0.146 | 0.122 | 0.110 |
(1)根据表中有关数据,你能推断出影响共价键键长的因素主要有哪些?_______。其影响的结果怎样?__________。
(2)通常,键能越__________,共价键越____,由该键构成的分子越稳定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】闪锌精矿(含有ZnS、SiO2和少量FeS杂质),钛白废液(含H2SO4约20%,还有少量Fe2+、TiO2+)。利用钛白废液及闪锌精矿联合生产七水合硫酸锌流程简化如下:

回答下列问题:
(1)在焙烧过程中,产生了具有漂白性的气体和金属氧化物,其中气体是_________,滤渣X的主要成分是_________________。
(2)氧化时,如果鼓入空气不足,其弊端是__________,生成H2TiO3的相关离子反应方程式为____________,从生产实际考虑,调pH时,选择加入石灰乳而不是烧碱的原因是_________。
(3)常温下,滤液Y中锌离子浓度约为6mol/L,若Ksp[Fe(OH)3]=4.0×10-38,Ksp[Zn(OH)2]=6.0×10-18。据此分析,加入石灰乳调节的pH应不超过________,此时溶液中还有的杂质阳离子为H+和__________。
(4)工业上,常用电解硫酸四氨合锌(II)溶液(含[Zn(NH3)4]2+)制备单质锌,其阴极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
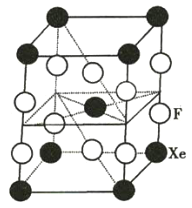
【题目】F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次增强),都极易与水反应。已知![]() ,下列推测正确的是( )
,下列推测正确的是( )
A.XeF2分子中各原子均达到8电子的稳定结构
B.某种氟化氙晶体的基本结构单元如图所示,可推知其化学式为XeF6
C.XeF4与水反应时,每生成2 mol Xe转移8 mol电子
D.XeF2加入水中,在水的作用下,将生成Xe和F2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 是四种短周期元素,
是四种短周期元素,![]() 、
、![]() 、
、![]() 同周期,
同周期,![]() 、
、![]() 同主族。
同主族。![]() 的原子结构示意图为
的原子结构示意图为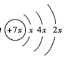 ,
,![]() 、
、![]() 形成的化合物的电子式为
形成的化合物的电子式为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.原子半径:![]()
B.电负性:![]()
C.原子序数:![]()
D.最高价氧化物对应水化物的酸性:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com