
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A����KIO3����������Һ�е�KI��5I����IO3-��3H2O=3I2��6OH��
B����NH4HSO3��Һ�мӹ�����NaOH��Һ�����ȣ�NH4+��OH��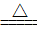 NH3����H2O
NH3����H2O
C��������SO2ͨ���䰱ˮ�У�SO2��NH3��H2O=HSO3-��NH4+
D��Ba(OH)2��Һ����μ���һ�����ʵ���Ũ�ȵ�NaHSO4��Һ������Һ�е�OH��ǡ�÷�Ӧһ��ʱ��Ba2����2OH����2H����SO42-=BaSO4����2H2O
 ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д�
ѧ�ڸ�ϰһ��ͨѧϰ�ܶ�Ա��ĩ������ӱ����������ϵ�д� â���̸����������������ϵ�д�
â���̸����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ�����и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ʺϵ�����������Ӧ2Fe3����2I��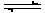 2Fe2����I2��Ƴ�����ͼ��ʾ��ԭ��ء������жϲ���ȷ����
2Fe2����I2��Ƴ�����ͼ��ʾ��ԭ��ء������жϲ���ȷ����
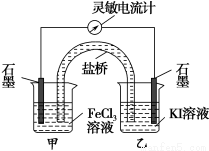
A����Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ
B����Ӧ��ʼʱ������ʯī�缫��Fe3������ԭ
C�������ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬
D�������ƶ���Ϊ����ڼ�������FeCl2���壬���е�ʯī�缫Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ������
���Ը�������Ҫ�ɷ���FeO��Cr2O3��������MgCO3��Al2O3��SiO2�ȣ�Ϊԭ����ȡNa2CrO4����Ĺ����������£�
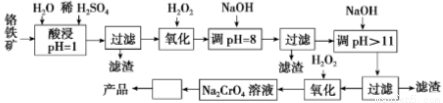
��֪����+3��Cr��������Һ�������ȶ�����pH>9ʱ��CrO ��ʽ���������������ڳ����£�����������������������ʽ����ʱ��Һ��pH���£�
��ʽ���������������ڳ����£�����������������������ʽ����ʱ��Һ��pH���£�
������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
��ʼ����ʱ��pH | 2.7 | 7.6 | 9.0 | ���� | ���� |
������ȫʱ��pH | 3.7 | 9.6 | 11.0 | 8 | 9��>9�ܽ⣩ |
��1��д�������е�2��ʹ��H2O2ʱ��������Ӧ�����ӷ���ʽ ��
��2������pH=8���͡���pH>11���м�ġ����ˡ������ܷ�ʡ�ԣ�Ϊʲô�� ��
��3������ͼ�д�Na2CrO4��Һ����Ʒ�м䡰�����ڵIJ����� ��
��4��CrO42-������������ת��ΪCr2O72-����ҵ�ϳ���Fe2+��������K2Cr2O7��ˮ���Ƚ�Cr2O72-ת��ΪCr3+���÷�Ӧ�����ӷ���ʽΪ ���ٵ�����Һ��pH= ��ʹ�����������ɳ�������ȥ��
��4�֣���1����֪��20��Cʱ��H2CO3��Ka1=4.2��10��7��Ka2=5.6��10��11��NH3•H2O��Kb=1.7��10��5��̼�������Һ��HCO3����NH4+��OH����H+��������Ũ���ɴ�С��˳��Ϊ
��2���ǰ���NH2OH���ɿ����ǰ������ڵ�1����ԭ�ӱ��ǻ�ȡ�������ʣ���������ԭ�������Գ�ȥ��Fe2+�е�Fe3+������������һ�������ȶ�������Ⱦ�����壬д����Ӧ�����ӷ���ʽ .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӵļ��鷽����ȷ����
A�������Һ���ȼ������ᱵ��Һ�а�ɫ�������ټ���ϡ���ᣬ��ɫ��������ʧ������ȷ�ϴ���Һ�к���SO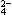
B�������Һ�м���NaOH��Һ�����ȣ�������������ʹʪ��ĺ�ɫʯ����ֽ����������ȷ�ϴ���Һ�к���NH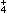
C�������Һ���ȼ�����ˮ���ٵ���KSCN��Һ����Һ��죬����ȷ�ϴ���Һ�к���Fe2+
D���ò�����պȡ����Һ���ھƾ��ƻ��������գ�����ʻ�ɫ������ȷ�ϴ���Һ�к���Na+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ�Ͳ��и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
25 ��ʱ�����и���������ָ����Һ��һ���ܴ����������
A����ǿ������Һ�У�Na����K����AlO2-��Cl��
B��pH��1����Һ�У�HCO3-��NH4+��NO3-��Ca2��
C����ɫ��Һ�У�Cu2����NO3-��Cl����H��
D����ɫ��Һ�У�Na����K����ClO����SO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ�Ͳ��и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�й�ʵ�����������ȷ����
A������һ�����ʵ���Ũ�ȵ���Һ������ʱ���ӻᵼ��������ҺŨ��ƫ��
B���ò�����պȡ��Һ������ʪ���pH��ֽ�ϲⶨ��Һ��pHֵ
C���� ��Һϴ�Ӳ����ղ�˿���ٽ�����ɫ��Ӧ
��Һϴ�Ӳ����ղ�˿���ٽ�����ɫ��Ӧ
D���ô����������������ƻ�̼����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ��Ԫ�и�����ѧ�ڵڶ��νβ����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���϶�һ�š�̽�������õ��������أ��为�������MΪ��������ԭ�ӵĺϽ𡣳��ʱ�缫��Ӧ�ֱ�Ϊ��M + H2O + e-= MH + OH-��Ni��OH��2 + OH-- e-= NiOOH + H2O��
�����й��������ص�˵����ȷ����
A���ŵ�ʱ������������pH��С
B���ŵ�ʱ���ܷ�ӦΪMH + NiOOH = M + Ni��OH��2
C�����ʱ���缫MӦ�����Դ��������
D�������������M�����MH��MH��HԪ����-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и�һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ����������������������ȷ����
A����״���£�22.4LH2O���еķ�����Ϊ1 NA
B�����³�ѹ��,����1.06g Na2CO3����Һ�к��е�Na+ ������Ϊ0.02 NA
C��ͨ��״���£�1 NA ��CO2����ռ�е����Ϊ22.4L
D�����ʵ���Ũ��Ϊ0.5mol/L��MgCl2��Һ�У�����Cl- ����Ϊ1 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ��һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ʵ�����ͬ�IJ�ͬ�������ϵ��
A����������һ�����
B������������
C����������ָ�����������
D������Ħ���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com