
【题目】下列溶液中溶质的物质的量浓度为1 mol/L的是( )
A. 将40gNaOH固体溶于1L水中
B. 将22.4 L氯化氢气体溶于水配成1L溶液
C. 将1L 10mol/L的浓盐酸与9L水混合
D. 将10g NaOH固体溶解在水中配成250 mL溶液
科目:高中化学 来源: 题型:
【题目】某化学实验小组为了验证SO2和Cl2的漂白性,设计了如下图所示的实验装置。请回答下列问题:
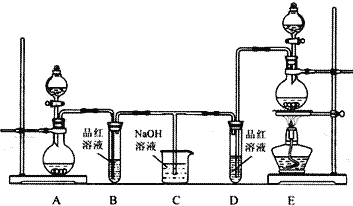
(1)他们制备SO2和Cl2所依据的原理分别是:Na2SO3+H2SO4═Na2SO4+H2O+SO2↑、MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,则上图A、E装置中用来制Cl2的装置是______(填序号),反应中盐酸所表现的性质是______性和______性,生成71gCl2转移的电子是______mol;
MnCl2+Cl2↑+2H2O,则上图A、E装置中用来制Cl2的装置是______(填序号),反应中盐酸所表现的性质是______性和______性,生成71gCl2转移的电子是______mol;
(2)反应开始后,发现B、D试管中的现象均为____________________________,停止通气后,给B、D两个试管中的溶液加热,B试管中的现象是________________________________;
(3)装置C的作用是____________________________________________________________;
(4)NaOH(足量)溶液与Cl2反应的离子方程式是__________________________________;
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见酸,因而失去漂白作用。该反应的化学方程式为______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算:
(1)用14.2g无水硫酸钠配制成500mL溶液,其物质的量浓度为____mol·L-1。
(2)若从中取出50mL,其物质的量浓度为____mol·L-1;溶质的质量为___g。
(3)若将这50mL溶液用水稀释到100mL,所得溶液中Na+的物质的量浓度为____mol·L-1,SO42-的物质的量浓度为_____mol·L-1。
(4)已知:a g某气体A含有b个分子,则c g该气体在标准状况下的体积为____ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g) ![]() 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A. 催化剂V2O5不改变该反应的逆反应速率
B. 保持容器体积不变,通入稀有气体增大反应体系的压强,反应速率一定增大
C. 该反应是放热反应,降低温度将缩短反应达到平衡的时间
D. 在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=(c2-c1)/(t2-t1)
查看答案和解析>>
科目:高中化学 来源: 题型:
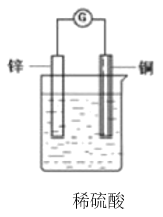
【题目】把一块锌片和一块铜片平行地插入盛有稀硫酸溶液的烧杯中,观察到的现象是________,再用导线把锌片和铜片连接起来,在导线中间接入灵敏电流计,灵敏电流计上观察到的现象是________;该原电池中电子流动的方向是________,总反应的化学方程式是________,其中________元素被氧化,________极上发生还原反应;在上述化学方程式上方用单线桥标出电子转移的方向和数目。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水中过量的氨氮(NH3和NH4+)会导致水体富营养化。某科研小组用NaClO氧化法处理氨氮废水。已知:①HClO的氧化性比NaClO强;②NH3比NH4+更易被氧化;③国家标准要求经处理过的氨氮废水pH要控制在6~9。
(1)pH=1.25时,NaClO可与NH4+反应生成N2等无污染物质,该反应的离子方程式为_____。
(2)进水pH对氨氮去除率和出水pH的影响如下图所示

①进水pH为1.25~2.75范围内,氨氮去除率随pH升高迅速下降的原因是_____
②进水pH为2.75~6.00范围内,氨氮去除率随pH升高而上升的原因是_____
③进水pH应控制在_____左右为宜。
(3)为研究空气对NaClO氧化氨氮的影响,其他条件不变,仅增加单位时间内通入空气的量,发现氨氮去除率几乎不变。其原因可能是_____(填字母)。
a.O2的氧化性比NaClO弱 b.O2氧化氨氮速率比NaClO慢
c.O2在溶液中溶解度比较小 d.空气中的N2进入溶液中
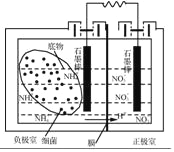
(4)利用微生物燃料电池可以对氨氮废水进行处理,其装置如图所示。闭合电路后,负极室与正极室均产生氮气,则负极室中NH4+发生反应的电极反应式为_____。该装置除了能对氨氮废水进行处理外,另一个突出的优点是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
B. 铁片与氯化铜溶液反应:Fe+Cu2+=Cu+Fe2+
C. 氢氧化镁溶于盐酸:Mg(OH)2+H+=Mg2++H2O
D. Cu(OH)2与稀硫酸反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某反应达平衡,平衡常数K=c(CO).c(H2O)/[c(CO2).c(H2)]。保持容器容积不变,升高温度,H2浓度减小,则下列说法不正确的是
A. 该反应的焓变为正值
B. 恒温恒容下,再充入CO2气体,H2浓度一定减小
C. 升高温度,会使正反应速率增大,逆反应速率减小,平衡正移
D. 该反应化学方程式为CO2+H2![]() CO+H2O
CO+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com