
【题目】500oC下,在2L体积固定的密闭容器中发生反应:2A(g)![]() 2B(g)+C(g)若开始时只充入2molA气体,达平衡时,混合气体的总物质的量为2.4mol。(作答此题时,要求写出计算过程)
2B(g)+C(g)若开始时只充入2molA气体,达平衡时,混合气体的总物质的量为2.4mol。(作答此题时,要求写出计算过程)
(1)计算500oC时该反应的化学平衡常数?
(2)平衡时A的转化率是多少?
(3)设温度不变,反应前容器内压强为p0,则反应达平衡时,容器内压强是多少?(用p0表示)
科目:高中化学 来源: 题型:
【题目】下列关于硅单质及其化合物的说法正确的是
①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维 ④陶瓷是人类应用很早的硅酸盐材料
A. ①② B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-==O2↑+4H+
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-==PO23-+3H2O
C.将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D.H3PO2溶于水的电离方程式为H3PO2![]() H++H2PO2-
H++H2PO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业中离子交换膜电解槽示意图如下图,其中的离子交换膜为“阳离子交换膜”,它有一特殊的性质:只允许阳离子通过,而阻止阴离子和气体通过。下列说法正确的是()
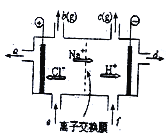
A. e口流入的是精制食盐水;f口流入的是蒸馏水
B. a口流出的是稀食盐水,d口流出的是氢氧化钠溶液
C. b为氯气,c为氧气
D. b与a口流出的溶液可制得漂白液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。请回答下列问题:
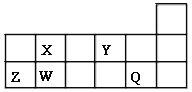
(1)W在周期表中的位置是___________,Y、Z的离子半径由大到小的顺序为___________ (用元素符号表示);由X与氢元素组成四原子化合物的电子式为__________。
(2)下列说法正确的是____________。
a.XY2和WY2都能溶于水生成对应的酸
b.Q的含氧酸的酸性比X的含氧酸的酸性强
c.X的最简单气态氢化物的稳定性大于W的最简单气态氢化物的稳定性
d.由NaOH溶液分别滴入MgQ2、ZQ3溶液中的反应现象可比较Mg和Z金属性的强弱
(3)自来水厂常用QY2对饮用水进行消毒,处理后的水中要求QY2的浓度在0.10~0.80 mg·L-1之间。碘量法可以检测水中QY2的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,再用NaOH溶液调至中性,并加入淀粉溶液,溶液变蓝。
操作Ⅱ:再加入一定量的Na2S2O3溶液。(已知:2S2O![]() +I2=S4O
+I2=S4O![]() +2I-)
+2I-)
操作Ⅲ:然后再加硫酸调节水样pH至1~3。
操作时,不同pH环境中Q元素粒子种类及化合价如图所示:
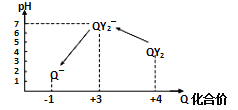
①操作Ⅰ中反应的离子方程式是_________________________。
②确定操作Ⅱ完全反应的现象是_________________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是______________________。
④若水样的体积为1.0 L,在操作Ⅱ中消耗了1.0×10-3mol·L-1的Na2S2O3溶液10 mL,则水样中QY2的浓度是_______________mg·L-1(精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向下列配合物的水溶液中加入AgNO3溶液,不能生成AgCl沉淀的是( )
A. [Co(NH3)3Cl3] B. [Co(NH3)6]Cl3
C. [Co(NH3)4Cl2]Cl D. [Co(NH3)5Cl]Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中有A、B两种物质,在一定的条件下反应:2A(气)+B(固)![]() 2C(气) △H>0达到平衡后,改变一个条件(X),下列量(Y)一定符合下图中曲线的是( )
2C(气) △H>0达到平衡后,改变一个条件(X),下列量(Y)一定符合下图中曲线的是( )

X | Y | |
A | 减小压强 | A的转化率 |
B | 升高温度 | 混合气体平均分子量 |
C | 升高温度 | A的浓度 |
D | 增加压强 | B的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学平衡移动的分析中,不正确的是( )
①已达平衡的反应C(s)+H2O(g)![]() CO(g)+H2(g),增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g),增大N2的浓度时,平衡一定向正反应方向移动
2NH3(g),增大N2的浓度时,平衡一定向正反应方向移动
③已达平衡的反应A(g)+B(g)![]() C(g)+D(g),升高温度,A的反应速率增大,则平衡一定正向移动
C(g)+D(g),升高温度,A的反应速率增大,则平衡一定正向移动
④已达平衡的反应H2(g) + I2(g) ![]() 2HI(g),恒压条件下充入氦气,平衡不移动
2HI(g),恒压条件下充入氦气,平衡不移动
A.①④ B.③④ C.①③ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
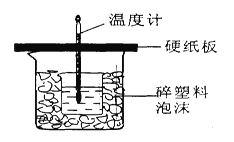
(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_____ _______。
(2)大烧杯上如不盖硬纸板,则求得的中和热数值___________(填“偏大”、“偏小’、“无影响”)
(3)实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,
与上述实验相比,所放出的热量____________(填“相等”或“不相等”),所求中和热的数值会____________(填“相等”或“不相等”),理由是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com