
| A、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B、Z在周期表中的位置为第3周期、IB族 |
| C、X的最高价氧化物对应水化物的酸性比W的弱 |
| D、W比Y更容易与氢气反应 |


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
| A、碳酸的酸性弱于盐酸,但强于次氯酸 |
| B、氯气通入草木灰的溶液中发生反应2K2CO3+Cl2+H2O═2KHCO3+KCl+KClO |
| C、氯气通入草木灰的溶液中发生反应K2CO3+Cl2+H2O═KHCO3+KCl+HClO |
| D、草木灰溶液本身不具有漂白作用,但具有去污作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
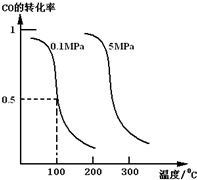 研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g).
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g).查看答案和解析>>
科目:高中化学 来源: 题型:
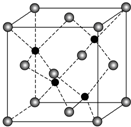 X、Y、Z、R、Q为前四周期元素,且原子序数依次增大,其中Y原子核外2p能级上有1个电子,R原子L层上有2对成对电子,X与Z可形成共价化合物ZX3,Q原子在第四周期中未成对电子数最多.请回答下列问题:
X、Y、Z、R、Q为前四周期元素,且原子序数依次增大,其中Y原子核外2p能级上有1个电子,R原子L层上有2对成对电子,X与Z可形成共价化合物ZX3,Q原子在第四周期中未成对电子数最多.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH3CH2Br
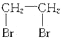 | |||||||
B、CH3CH2Br
| |||||||
C、CH3CH2Br
| |||||||
D、CH2=CH2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氟酸刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O |
| B、明矾用于净水:Al3++3H2O=Al(OH)3+3H+ |
| C、纯碱去除油污:CO32-+H2O?HCO3-+OH- |
| D、氯气制备“84”消毒液:Cl2+2OH-=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
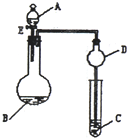 用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com