
【题目】下列叙述正确的是
A. 1 摩尔任何物质都含有 6. 02×1023 个分子
B. 摩尔是国际单位制中 7 个基本物理量之一
C. 含有 6.02×1023 个氧原子的H3PO4的物质的量是 0.25mol
D. 氧气的摩尔质量等于它的相对原子质量
科目:高中化学 来源: 题型:
【题目】化学知识中有很多的“相等”。下列叙述正确的是( )
A. 原子中原子核内的质子数和中子数一定相等
B. 同种元素的原子和离子核外电子数相等
C. 化学反应前后,同种元素的原子数目一定相等
D. 把一定量的食盐放入水中,得到溶液的质量与食盐和水的总质量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据同分异构体的概念,判断下列物质互为同分异构体的是( )
A.CH3﹣CH2﹣NO2 和 H2N﹣CH2﹣COOH
B.H和D
C.甲烷和正丁烷
D.红磷和白磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向59.2 g Fe2O3和FeO的混合物中加入某浓度的稀硝酸1.0 L,固体物质完全反应,生成NO和Fe(NO3)3。在所得溶液中加入1.0 mol/L的NaOH溶液2.8 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为85.6 g。下列有关说法错误的是( )
A.Fe2O3与FeO的物质的量之比为1∶6
B.硝酸的物质的量浓度为3.0 mol/L
C.产生的NO在标准状况下的体积为4.48 L
D.Fe2O3,FeO与硝酸反应后剩余HNO3为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,4个容器中分别装有4种气体,已知各容器中的气体和容器的容积分别是a.CO2 100 mL;b.O2200 mL;c.N2 400 mL;d.CH4 600 mL,则4个容器中气体的质量由大到小的顺序是
A. a>b>c>d B. b>a>d>c C. c>d>b>a D. d>c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度为c mol/L,体积为V mL的AgNO3溶液分别与100 mL NaCl、MgCl2、AlCl3溶液恰好完全反应,则这三种溶液的物质的量浓度之比为
A.6∶3∶2 B.1∶2∶3 C.2∶3∶6 D.2∶6∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿主要含Ca5(PO4)3F和CaCO3·MgCO3 。某研究小组提出了磷尾矿综合利用的研究方案,制备具有重要工业用途的CaCO3、Mg(OH)2、P4和H2,其简化流程如下:
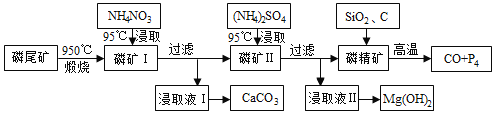
已知:①Ca5(PO4)3F在950℃不分解;
②4Ca5(PO4)3F+18SiO2+30C![]() 2CaF2+30CO+18CaSiO3+3P4
2CaF2+30CO+18CaSiO3+3P4
(1)950℃煅烧磷尾矿生成气体的主要成分是___________。
(2)实验室过滤所需的玻璃仪器是_____________。
(3)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是__________。
(4)在浸取液II中通入NH3,发生反应的化学方程式是____________。
(5)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
5CaO(s)+H3PO4(l)+HF(g)=Ca5(PO4)3F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小,下列说法正确的是
。恒容时,温度升高,H2浓度减小,下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为CO+H2O![]() CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG)。这两类燃料的主要成分都是( )
A. 碳水化合物 B. 烃类 C. 氢气 D. 醇类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com