
| n |
| V |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
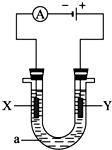 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请完成以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 30mL盐酸 | 30mL盐酸 | 30mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
| A、向50 mL盐酸中加入混合物27.6 g时,盐酸过量 |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、15.7 g混合物与盐酸恰好能完全反应 |
| D、盐酸的物质的量浓度为5.0 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na→NaOH |
| B、Al2O3→Al(OH)3 |
| C、Fe→FeCl2 |
| D、Fe(OH)2→Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
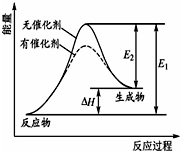 某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂能改变反应的焓变 |
| C、催化剂能降低反应的活化能E1和 E2 |
| D、增大反应物的浓度,可使单位体积内活化分子百分数增大,反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(SCN)3溶液中存在Fe3++3SCN- Fe(SCN)3,向此溶液中加入固体KSCN后颜色变深 |
| B、用通过盛饱和食盐水的洗气瓶来除去氯气中的少量HCl气体杂质 |
| C、反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
| D、合成氨:N2(g)+3H2(g)?2NH3 (g)△H<0在高温、高压和催化剂条件下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入大量水稀释时,平衡向右移动,溶液中c(H+)减小 |
| B、加入几滴浓盐酸,平衡向左移动,溶液的pH值增大 |
| C、加入几滴浓氨水,平衡向逆反应方向移动,c(OH-)减小 |
| D、升温至35℃,平衡向右移动,NH4Cl的水解程度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、200 mL 1 mol?L-1NaCl溶液 |
| B、50 mL 0.5 mol?L-1AlCl3溶液 |
| C、100 mL 0.8 mol?L-1MgCl2溶液 |
| D、200 mL 2 mol?L-1KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜与稀硝酸的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| B、氯气与水反应:Cl2+H2O=H++Cl-+HClO |
| C、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、钠和水反应:2Na+H2O=2Na++2OH-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com