
| 5 |
| 8 |
| m |
| ρ |
| 16×36.5×15.8g |
| 2×158 |
| 29.2g |
| 36.5% |
| 5 |
| 8 |
| 5 |
| 8 |
| 15.8g×5×71 |
| 2×158 |
| 17.75g |
| 3.17g/L |


科目:高中化学 来源: 题型:
| A、HX | B、HY |
| C、MOH | D、NOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
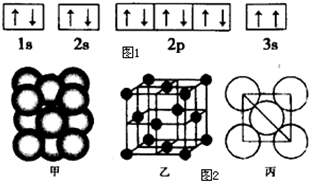 现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.| A原子的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol, |
| D原子核外所有P轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠能和大多是非金属单质直接化合,生成其相应的化合物 |
| B、钠能与水反应实际上是与水电离产生的H+的反应 |
| C、钠在水溶液中参加的反应,都是先与水反应 |
| D、钠不能置换出盐中的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 根据Fe3++Ag?Fe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去.
根据Fe3++Ag?Fe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去.- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
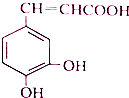
| A、该物质中苯环上一氯代物有2种 |
| B、1mol该物质可以与1.5mol碳酸钠溶液反应生成1.5mol的CO2 |
| C、既能发生取代反应,也能发生加成反应 |
| D、所有碳原子不可能都在同一平面上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com