
| A����̼��������Һ�м������������������Һ��Ca2++HCO3-+OH-=CaCO3��+H2O |
| B����������Һ�м���������Ba��OH��2��Һ��Al3++3OH-+Ba2++SO42-=BaSO4��+Al��OH��3�� |
| C����Fe2��SO4��3��Һ�м��������Na2S��2Fe3++S2-=2Fe2++S�� |
| D������1molFeBr2��Һ��ͨ���״����22.4L��Cl2��2Br-+Cl2=Br2+2Cl- |


 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
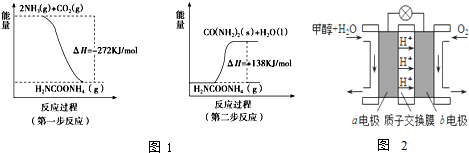
| �¶ȣ��棩 | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol Cl2��Ϊ�������õ��ĵ�����ΪNA |
| B��22.4 L CH4���е�ԭ����Ϊ5 NA |
| C��14 g N2���е�ԭ����ΪNA |
| D��3 mol Fe�������������ַ�Ӧ��ת��9NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol CO2 ������Ϊ44g/mol |
| B��Ħ���DZ�ʾԭ�ӡ����ӡ����Ӹ����ĵ�λ |
| C��64g�������2mol�� |
| D��NA��CO2����������gΪ��λ����CO2��Ħ����������ֵ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Cu��FeCl3��Һ��Ӧ��Cu+2Fe3+=2Fe2++Cu2+ |
| B������ϡH2SO4��Ӧ��2Fe+6H+=2Fe3++3H2�� |
| C����AlCl3��Һ�е������NaOH��Һ��Al3++3OH-=Al��OH��3�� |
| D��Na��ˮ��Ӧ��Na+2H2O=Na++2OH-+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ �ռ� С�մ� |
| B������ ���� ���� |
| C������ �ƾ� ʯ��ʯ |
| D������ ��ʯ�� ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
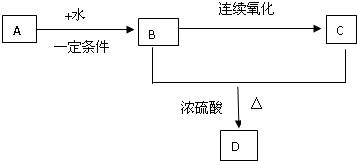
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 U��V��W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪U��һ�ֺ��ص�������Ϊ14��������Ϊ7��V��������NH
U��V��W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪U��һ�ֺ��ص�������Ϊ14��������Ϊ7��V��������NH+ 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | HA���ʵ���Ũ�ȣ�mol/L�� | NaOH���ʵ���Ũ�� ��mol/L�� | �����Һ��PH |
| �� | 0.2 | 0.2 | a |
| �� | c1 | 0.2 | 7 |
| �� | 0.2 | 0.1 | 7 |
| �� | 0.1 | 0.1 | 9 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com