

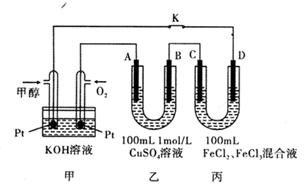
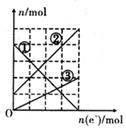
| A.装置①中阳极上析出红色固体 |
| B.装置②中铜片应与电源负极相连 |
| C.装置③中外电路电流方向:b极 →a极 |
| D.装置④中阴极反应:2 Cl--2e-= Cl2 |
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:不详 题型:填空题
| A.铜 | B.钠 |
| C.锌 | D.石墨 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
2Ni(OH)2。根据此反应式,下列 有关说法中正确的是: 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.纯银器表面在空气中因电化学腐蚀而渐渐变暗 |
| B.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| C.钢柱在水下部分比在空气与水交界处更容易腐蚀 |
| D.当镀锌铁制品的镀层受损后,镀层仍能对铁制品起保护作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
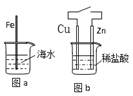
| A.图a,负极上发生的反应是:O2+4e+2H2O → 4OH- |
| B.图b,接通开关后溶液中的H+向正极移动 |
| C.图a,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D.图b,接通开关后Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
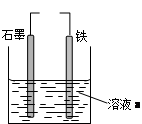
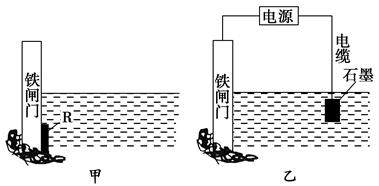
| A.若两电极直接连接,a是食盐水,则发生析氢腐蚀 |
| B.若两电极直接连接,则电子从铁流向石墨 |
| C.若铁接电源负极,石墨接电源正极,a是稀H2SO4溶液,电解一段时间后溶液的pH增大 |
| D.若铁接电源正极,石墨接电源负极,a是氯化铜溶液,阴离子向石墨电极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
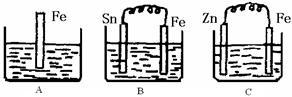
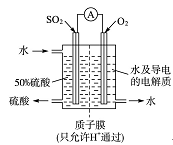
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com