
【题目】过碳酸钠(2Na2CO3·3H2O2)广泛用于化工、造纸、纺织、食品等行业,一种以芒硝(Na2SO4·10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如下:
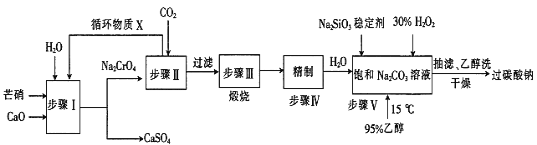
已知:2CrO42-+2H+![]() Cr2O72-+H2O,pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。回答下列问题:
Cr2O72-+H2O,pH小于5时几乎均以Cr2O72-形式存在,pH大于8.5时几乎均以CrO42-形式存在。回答下列问题:
(1)由步骤I可知:Ksp(CaCrO4)_____Ksp(CaSO4)(填“>”或“<”)。
(2)流程中循环物质X的主要溶质为____________(填化学式)。
(3)步骤II后的溶液过滤得到一种酸式盐固体,其发生反应的离子方程式为________________。
(4)步骤III是为了制得纯碱,其化学方程式为 _________________________________。
(5)步骤V合成时,调节温度为15℃并加入95%乙醇的目的是____________________。
(6)测定产品活性氧的实验步骤如下:准确称取mg产品,用硫酸溶解后,用c mol· L-1的KMnO4标准溶液滴定至终点,消耗KMnO4标准溶液V mL。
①该滴定过程不需要外加指示剂的原因是_________________________________ 。
②滴定到终点时,溶液最终呈________(填“无色”或“浅红色”)。
【答案】> Na2Cr2O7 2Na++2CrO42-+2CO2+H2O=Cr2O72-+2NaHCO3↓ 2NaHCO3![]() Na2CO3+CO2↑+H2O↑ 减小过碳酸钠溶解度,促使其析出 KMnO4溶液本身有紫红色 浅红色
Na2CO3+CO2↑+H2O↑ 减小过碳酸钠溶解度,促使其析出 KMnO4溶液本身有紫红色 浅红色
【解析】
本题是一道工业流程题,用芒硝来制备过碳酸钠,据此来分析即可。步骤I分离出了不溶于水的![]() ,因此是过滤;步骤II向溶液中通入
,因此是过滤;步骤II向溶液中通入![]() 是为了得到
是为了得到![]() ,另一方面由于
,另一方面由于![]() 的水溶液为弱酸性,溶液中的铬元素以
的水溶液为弱酸性,溶液中的铬元素以![]() 的形式存在,因此溶液中还有
的形式存在,因此溶液中还有![]() ,可以循环利用。
,可以循环利用。![]() 在水中的溶解度不大,因此过滤后煅烧得到
在水中的溶解度不大,因此过滤后煅烧得到![]() ,碳酸钠精制后加水得到饱和碳酸钠溶液,再和双氧水进行氧化还原即可。加入95%乙醇的目的是为了降低产物的溶解度,使产物析出,本题得解。
,碳酸钠精制后加水得到饱和碳酸钠溶液,再和双氧水进行氧化还原即可。加入95%乙醇的目的是为了降低产物的溶解度,使产物析出,本题得解。
(1)根据沉淀的转化,溶解度高的沉淀可以转化为溶解度低的沉淀,因此![]() 大于
大于![]() ;
;
(2)根据分析,物质X为![]() ;
;
(3)根据分析,步骤II是通过通入![]() 来得到
来得到![]() ,此处的
,此处的![]() 因溶解度较低析出,使反应得以发生:
因溶解度较低析出,使反应得以发生:![]() ;
;
(4)煅烧![]() 使其分解即可得到纯碱:
使其分解即可得到纯碱:![]()
![]()
![]() ;
;
(5)根据分析,降温和加入极性介质均可降低产物在溶液中的溶解度,方便收集;
(6)①在做高锰酸钾相关的滴定时一般不需要加指示剂,因为高锰酸钾本身具有明显的紫红色 ;
②当达到滴定终点后,溶液中的活性氧已被消耗完,此时若再滴入高锰酸钾,就会过量,过量的高锰酸钾呈浅红色。


科目:高中化学 来源: 题型:
【题目】实验室制取的乙烯中常混有少量的![]() ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
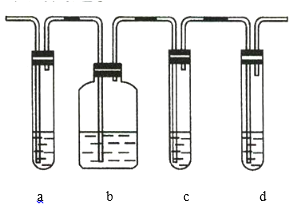
(1)图中a、b、c、d装置盛放的试剂依次是___________________(填序号)。
A.品红溶液 B.![]() 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明![]() 存在的实验现象是______________________________________。
存在的实验现象是______________________________________。
(3)使用装置b的目的是________________________。
(4)使用装置c的目的是________________________。
(5)能说明混合气体中含有乙烯的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇烃化新技术是近几年合成氨工业净化精炼原料气,除去少量CO一种新方法,其原理可分为甲醇化与甲烷化两个部分。
甲醇化:![]()
![]()
甲烷化:![]()
![]()
![]() 下列措施有利于提高醇烃化过程CO转化率的是________。
下列措施有利于提高醇烃化过程CO转化率的是________。
A.及时分离出![]() 适当升高反应温度
适当升高反应温度
C.使用高效的催化剂 ![]() 适当增大压强
适当增大压强
![]() 甲醇化平衡常数可用
甲醇化平衡常数可用![]() 表示,
表示,![]() 为平衡组分中各物质的物质的量分数。若CO与
为平衡组分中各物质的物质的量分数。若CO与![]() 混合原料气中CO的体积分数为
混合原料气中CO的体积分数为![]() ,经甲醇化后CO的平衡转化率为w,则
,经甲醇化后CO的平衡转化率为w,则![]() ________
________![]() 用含w的表达式来表示
用含w的表达式来表示![]() 。
。
![]() 测试a、b两种催化剂在不同压强与温度条件下,甲醇化过程中催化效率如下图:
测试a、b两种催化剂在不同压强与温度条件下,甲醇化过程中催化效率如下图:

从上图可知选择哪种催化剂较好________![]() 填a或
填a或![]() ,理由是________。
,理由是________。
![]() 下列关于醇烃化过程说法正确的是________。
下列关于醇烃化过程说法正确的是________。
A.甲醇化与甲烷化过程在任何条件下均为自发反应
B.选择不同的催化剂可以控制醇烃化过程中生成甲醇与甲烷的百分含量
C.当温度与反应容器体积一定时,在原料气中加入少量的惰性气体,有利于提高平衡转化率与甲醇的产率
D.适当增大混合气体中![]() 的百分含量,有利于提高醇烃化过程CO平衡转化率
的百分含量,有利于提高醇烃化过程CO平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有图1、2所示的装置,下列叙述正确的是( )


图1 图2
A.将乙烯分别通入两个装置中,二者都褪色且原理相同
B.若某气体均能使二者褪色,说明该气体一定含乙烯
C.二者都可用于除去乙烷中混有的乙烯
D.二者都可用于鉴别乙烷和乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃在标准状况下的密度为3.215 g/L,现取3.6 g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4 g,碱石灰增重11 g,求:
(1)该烃分子的摩尔质量。
(2)确定该烃的分子式。
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素是只含碳、氢、氧三元素的有机物,是高效的抗疟药,为无色针状晶体,易溶于乙醚中,在水中几乎不溶,熔点为156~157℃,已知乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础,以乙醚浸取法的主要工艺如图所示:回答下列问题:
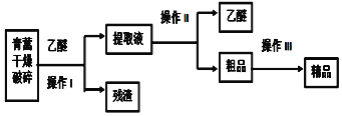
(1)选用乙醚浸取青蒿素的原因是______。
(2)操作Ⅰ需要的玻璃仪器主要有:烧杯、玻璃棒和______,操作Ⅱ的名称是______,操作Ⅲ利用青蒿素和杂质在同一溶剂中的溶解性差异及青蒿素溶解度随温度变化较大的原理提纯,这种方法是______。
(3)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成,如图所示的是用燃烧法确定青蒿素分子式的装置:
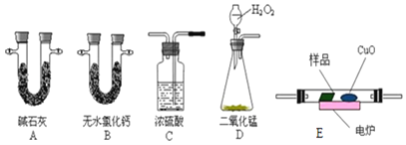
①按上述所给的测量信息,装置的连接顺序应是______。(装置可重复使用)
②青蒿素样品的质量为28.2g,用连接好的装置进行试验,称得A管增重66g,B管增重19.8g,则测得青蒿素的最简式是______。
③要确定该有机物的分子式,还必须知道的数据是______,可用______仪进行测定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃)。下列说法不正确的是
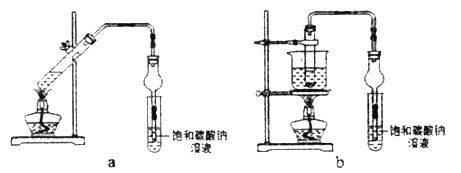
A. 浓硫酸能加快酯化反应速率 B. 不断蒸出酯,会降低其产率
C. 装置b比装置a原料损失的少 D. 可用分液的方法分离出乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,三个等体积的干燥圆底烧瓶中分别充满①HCl;②NO2;③体积比为4:1的NO2和O2,进行喷泉实验。经充分反应后烧瓶内溶质的物质的量浓度之比为( )
A.1:1:1B.4:4:5C.5:5:4D.15:10:12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知海水提取镁的主要步骤如下:
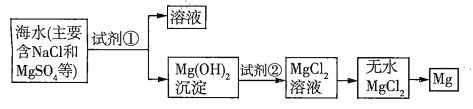
(1)关于加入试剂①作沉淀剂,有以下方法,请完成下列问题。
方法 | 是否合理 | 简述理由 |
方法:高温加热蒸发海水后,再加入沉淀剂 | a | b |
你认为合理的其他方法是c |
a. _____________;
b.____________;
c.____________。
(2)框图中加入的试剂①应该是_______(填物质名称),加入试剂②的溶质是_______(填化学式)。工业上由无水![]() 制取镁的化学方程式为___________。
制取镁的化学方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com