
【题目】一定温度下,两个恒容密闭容器中分别发生反应:
①H2(g)+I2(g)![]() 2HI(g);
2HI(g);
②C(s)+H2O(g)![]() CO(g)+H2(g),
CO(g)+H2(g),
下列状态能表明两反应都达到平衡状态的是
a.各物质的浓度不变;b.容器内气体压强不变;c.容器内气体密度不变;d.容器内气体颜色不变;e.各组分的物质的量分数或质量分数不变;f.混合气体的平均分子量不变;
A. ae B. aef C. abc D. ac
【答案】A
【解析】试题分析:a.各物质的浓度不变,说明①②中各物质的量不变,都达平衡状态,a正确;b.容器内气体压强不变,①压强始终不变,所以压强不变无法判断①是否达到平衡状态,b错误;c.容器内气体密度不变,由于①反应的两边气体的体积相同且都是气体,容器的容积不变,所以密度始终不变,无法判断①是否达到平衡状态,c错误;d.容器内气体颜色不变,由于②反应容器内气体颜色始终不变,d错误;e.各组分的物质的量分数或质量分数不变,说明①②中各物质的量不变,都达平衡状态,e正确;f.混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,由于①反应的两边气体的体积相同且都是气体,所以混合气体的平均分子量不变不能说明反应达到平衡状态,f错误。答案选A。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 18 g H2O中含有10NA个质子
B. 1 mol甲苯中含有6NA个C—H键
C. 标准状况下,22.4 L氨水中含有NA个NH3分子
D. 将56 g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5L 2mol/L FeCl3溶液与0.2L 5mol/L KCl溶液中的Cl﹣物质的量之比( )
A.6:5
B.3:2
C.15:2
D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一体积为10 L的容器中,通入一定量的CO和H2O,在850 ℃时发生如下反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g);ΔH<0。CO和H2O浓度变化如图,则0~4 min的平均反应速率v(CO)=____ mol/(L·min)。
CO2(g)+H2(g);ΔH<0。CO和H2O浓度变化如图,则0~4 min的平均反应速率v(CO)=____ mol/(L·min)。
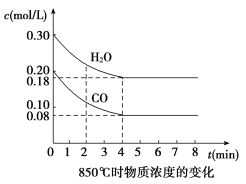
t1 ℃时物质浓度(mol/L)的变化
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
(2)t1 ℃(高于850 ℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。请回答:
①表中3~4 min之间反应处于________状态;c1数值________0.08 mol/L(填大于、小于或等于)。
②反应在4~5 min间,平衡向逆方向移动,可能的原因是________(单选),表中5~6 min之间数值发生变化,可能的原因是________(单选)。
a.增加了水蒸气的量 b.降低温度
c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
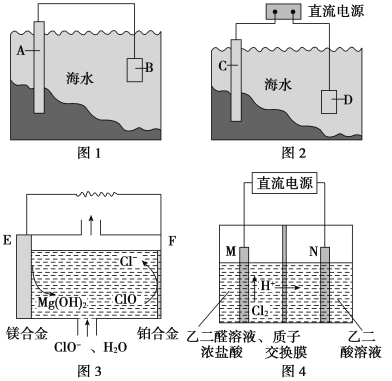
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择____________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:_________________________。
(2)图2中,钢闸门C做____________极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为____________,检测该电极反应产物的方法是___________________。
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁﹣次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的__________极(填“正”或“负”)。F电极上的电极反应式为________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_______________________。
(4)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为____________________________。
②若有2 mol H+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一可逆反应2A(g)+3B(g)![]() 4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是
4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是
A.前20 min的平均反应速率v(C)=0.1 mol/(Lmin) B.A的转化率为50%
C.C的平衡浓度c(C)=4 mol/L D.B的平衡浓度c(B)=1.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基态Fe原子有________个未成对电子。Fe3+的电子排布式为________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com