
【题目】工业上常用加入K2Cr2O7氧化剂的办法氧化Na2SO3,现已知1mol K2Cr2O7能把3 mol Na2SO3恰好氧化为Na2SO4,K2Cr2O7被还原为Crn+,则n的值为
A. +2 B. +3 C. +4 D. +5
 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】反应NH4HS(s) ![]() NH3+H2S(g)在一定温度下达到平衡。下列各种情况下,不能使平衡发生移动的是
NH3+H2S(g)在一定温度下达到平衡。下列各种情况下,不能使平衡发生移动的是
①温度、容积不变时,通入SO2气体 ②移走一部分NH4HS固体
③容积不变,充入氮气 ④充入氮气,保持压强不变
A. ①② B. ①③ C. ①②③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假如生长激素由两条多肽链组成,在生长激素的缩合过程中脱掉的水分子相对分子质量为3 384,已知20种氨基酸的平均分子质量为130,此蛋白质的分子量最接近于 ( )
A. 24 700 B. 21 316 C. 24 440 D. 440180
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《化学与生活》模块试题
(1)我国农业因遭受酸雨而造成的损失每年高达15亿多元,酸雨是指pH小于________的雨水,这主要是由人为排放的_______和________(填元素名称)的氧化物等酸性气体转化而成的。为治理酸雨的影响,可将CaCO3粉末撒到受酸雨影响的湖泊中,若用离子方程式表示该反应的本质,请完成如下离子反应:CaCO3+2H+==_____________________________。
主食 | 米饭 |
副食 | 红烧鱼 |
饮品 | 豆浆 |
配菜 | ? |
(2)“民以食为天”,人类生命活动所需的各种营养物质主要来自食物。上表制定的食谱中,主食含有的基本营养物质主要是__________,副食含有的基本营养物质主要是_____________;豆浆所属的分散系为__________________。考虑营养成分的均衡搭配,应补充的配菜是__________________。
(3)水是一种宝贵的自然资源。
①生活污水中,经常包括含__________、___________(填元素符号)的化合物,会造成水体植物营养物质污染。水中的氨在微生物的作用下,可被氧化成HNO2,进而氧化成HNO3,写出这一过程的化学方程式____________________________。
②氧化还原法是处理污水常用的方法。某地工厂排放的污水,经检测,污水中含有0.012 mol/L的游离溴,可用Na2SO3还原除去污水中的溴,请写出其化学方程式:___________________________;处理5 L这种污水,至少需加入0.05 mol/L的 Na2SO3 溶液________L才能将溴全部除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
A.XYZ2 B.X2YZ3 C.X2YZ2 D.XYZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列有关说法中正确的是
A. 草木灰溶液呈碱性,不能与铵态氮肥混合施用
B. 漂白粉中Ca(ClO)2具有强氧化性,能用来净化水
C. 碳纳米管是新型有机合成纤维,可用作储氢材料
D. 为防止食品腐败可在其包装袋里放置硅胶颗粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法正确的是( )
A. 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B. 将钠投入到盛满水的烧杯中,观察钠与水反应实验现象
C. 制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D. 实验室配制一定浓度NaOH溶液,将称量固体溶解后马上转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素在生活中有广泛应用,根据所需知识回答下列问题。
(1)氟元素基态原子的价电子排布图:_________,卤族元素位于元素周期表______区。
(2)在一定浓度的氢氟酸溶液中,部分溶质以二分子缔合(HF)2形式存在,使HF分子缔合的作用力是_______________。
(3)BF3常温下是气体,有强烈的接受弧电子对的倾向。BF3分子的立体构型为______,固态时的晶体类型是_______,BF3与NH3相遇立即生成白色固体,写出该白色固体物质的结构式并标注出其中的配位键_____。
(4)根据下表提供的数据判断,熔点最高、硬度最大的是_______(填化学式)。
离子晶体 | NaF | MgF2 | AlF3 |
晶格能(KJ·mol-1) | 923 | 2957 | 5492 |
(5)已知NaClO2晶体中阴离子为V型,ClO2-中氯原子的弧电子对数是______,ClO2-中氯原子的杂化轨道类型为_____,HClO4比HClO2酸性强的原因是_______。
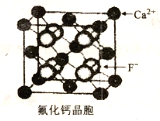
(6)CaF2晶胞如下图所示。已知:NA为阿伏伽德罗常数,棱上相邻的两个Ca2+的核间距为acm,则CaF2的密度可表示为_____g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com