
【题目】TiS2是镁电池的重要组成材料,其制备原理为Ti(SO4)2+8H2=TiS2+8H2O。下列说法正确的是
A. Ti(SO4)2失去电子B. H2被还原
C. H2是氧化剂D. Ti(SO4)2被还原
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】工业上用H2和N2直接合成氨:N2+3H2=2NH3,下列措施肯定能使合成氨反应速率加快的是:
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④增大压强
A.只有①②③ B.只有①②④ C.只有①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法正确的是( )
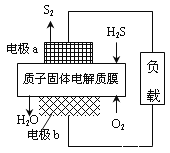
A. 电池工作时,电流从电极a经负载流向电极b
B. 电极a上发生的电极反应为:2H2S - 4e-=S2 + 4H+
C. 当反应生成64gS2时,电池内部释放632kJ热能
D. 当电路中通过4mol电子时,有4molH+经质子膜进入负极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各有机物的说法不正确的是
A. 乙烯可使溴的四氯化碳溶液褪色B. 乙醇可与金属Na发生置换反应
C. 苯可使酸性KMnO4溶液褪色D. 乙酸的酸性比碳酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表1是元素周期表的一部分:
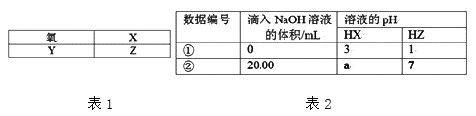
25℃时,用浓度为0.1000 mol/L的氢氧化钠溶液分别滴定20.00mL浓度均为0.1000 mol/L的两种酸HX、HZ(忽略体积变化),实验数据如表2,下列判断正确的是
A. 表格中a<7
B. HX和HZ等体积混合后pH=1+lg2
C. Y和Z两元素的简单氢化物受热分解,前者分解温度高
D. 0.l000mol/LNa2Y的水溶液中:c(Y2—)+c(HY—)+c(H2Y)=0.1000mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH3→CH3CH2Cl→CH2 = CH2→CH3CH2OH的转化过程中,经过的反应是
A.取代→消去→加成 B.裂解→取代→消去
C.取代→加成→氧化 D.取代→消去→水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。下列关于海洋氮循环的说法正确的是
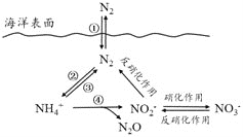
A. 海洋中的氮循环起始于氮的氧化
B. 海洋中的氮循环属于固氮作用的是③
C. 海洋中的反硝化作用一定有氧气的参与
D. 向海洋排放含NO3—的废水会影响海洋中NH4+的含量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com