
【题目】(1)有一种金属单质A,焰色反应颜色呈黄色,能发生下图所示变化:

上图中淡黄色固体B是_____________填化学式)
(2)钠的化合物中,可用于呼吸面具作为O2来源的是______
(3)写出(1)中C溶液与硝酸反应的化学方程式:______
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)26H2O,相对分子质量392]晶体又称莫尔盐,易溶易电离但却比一般的亚铁盐稳定,因此广泛应用于制药、电镀以及定量分析。回答下列与之有关的问题:
(1)在莫尔盐所涉及的五种元素中:
①S元素在门捷列夫元素周期表中的位置是 ______________ ;
②其中处于同主族的两种元素非金属性更强的是:_____________。
(2)为检验莫尔盐是否变质,可用的试剂为_______________。
碘是合成人体甲状腺激素的重要原料,食盐中加KIO3是我国为解决普遍性碘缺乏问题的国家规定,下图是自动电位滴定法测定食盐中碘含量的实验过程:
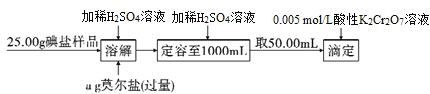
(3)已知“溶解”过程中IO3-的还原产物为碘单质,写出该反应的离子反应方程式:______________________________。
(4)取50. 00 mL样品,用0.005 mol/L酸性K2Cr2O7溶液滴定剩余Fe2+,滴定操作时使用的锥形瓶未干燥,导致结果_____________(填“偏大”“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸![]() 是一种有机物,它在多种生物化学过程中起重要作用。
是一种有机物,它在多种生物化学过程中起重要作用。
(1)乳酸分子中含有的官能团有________________(填写官能团名称)。
(2)1.5 mol乳酸与足量的Na反应生成氢气在标准状况下的体积是______L。
(3)当乳酸与浓硫酸共热时,能产生多种酯类化合物,其中有一种六元环状酯,写出其结构简式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用如图装置,进行NH3与金属氧化物MxOy反应生成M、N2、H2O,通过测量生成水的质量来测定M的相对原子质量。a中试剂是浓氨水。

①仪器a的名称为_________,仪器b中装入的试剂可以是___________。
②按气流方向正确的装置连接顺序为_________(填字母,装置可重复使用)。
(2)亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
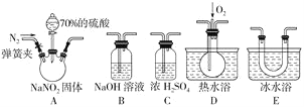
已知:ⅰ.NO+NO2+2OH-=2NO2-+H2O
ⅱ.气体液化的温度:NO2(21℃)、NO(-152℃)
①反应前应打开弹簧夹,先通入一段时间氮气,目的是________________。
②为了检验装置A中生成的气体产物,仪器的连接顺序(从左向右连接):A→_________;组装好仪器后,接下来进行的操作是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。下列说法不正确的是
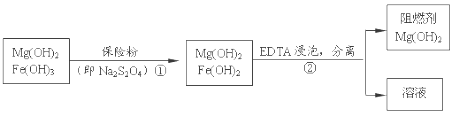
A. 步骤②中分离操作的名称是过滤,Mg(OH)2可以作阻燃剂是因为它分解需要吸收大量的热
B. 步骤①中的反应式:3Fe(OH)3 +S2O42-+2OH- =3Fe(OH)2 +2SO42-+4H2O
C. 步骤①中保险粉是作还原剂
D. 从步骤② 中可知OH- 和EDTA共存时,Fe2+更易和EDTA结合,生成可溶性化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组,拟探究和比较SO2和C12的漂白性, 设计如下图所示的实验装置二套。请你参与探究并回答下列问题。
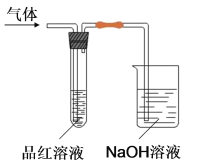
(1)向第一套装置中通入一段时间的SO2,观察到试管中的品红溶液褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12,观察到试管中的品红溶液也褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理____(填“相同”或“不相同”);
(4) C12通入品红溶液中,生成的具有漂白性的物质是_____(填“HC1”或“HClO”)。
(5)烧杯中NaOH溶液的作用是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,两电极上发生的电极反应为a极:Cu2++2e-=Cu;b极:Fe-2e-=Fe2+。下列说法不正确的是
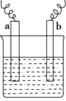
A.电解质溶液含有Cu2+
B.该装置是化学能转化为电能
C.a、b可能是同种电极材料
D.a极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何综合利用有毒的NO2气体一直是科研的热门话题,根据反应4NO2+O2=2N2O5,有些科学家设计了如图所示的燃料电池,下列相关说法正确的是
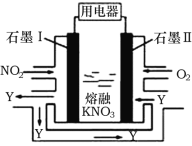
A.图示中Y为NO,可以循环利用
B.电池工作过程中,NO3-向石墨Ⅰ电极迁移
C.正极发生的反应为NO+O2+e- =NO3-
D.转移1 mol电子时,负极产物为0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年3月21日是第二十七届“世界水日”,保护水资源,合理利用废水节省水资源,加强废水的回收利用已被越来越多的人所关注。已知:某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100![]() ,进行了三组实验,其操作和有关图像如下图所示,请回答下列问题:
,进行了三组实验,其操作和有关图像如下图所示,请回答下列问题:
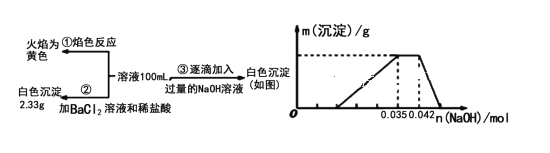
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是_______,一定存在的阳离子是____________________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:_________________________。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为__________,所得沉淀的最大质量是__________g。
(4)若通过实验确定原废水中c(Na+)=0.14mol/L,试判断原废水中NO3-是否存在?__________(填“存在”“不存在”或“不确定”)。若存在,c(NO3-)=__________mol/L。(若不存在或不确定则此空不填)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com