
����Ŀ����֪t ��ʱAgCl��Ksp��4��10��10����t ��ʱ��Ag2CrO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������(����)
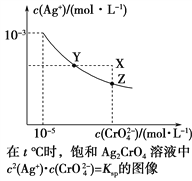
A. ��t ��ʱ��Ag2CrO4��KspΪ1��10��11
B. �ڱ�����Һ�м���K2CrO4(s)��ʹ��Һ��Y�㵽Z��
C. ��t ����Ag2CrO4(s)��2Cl��(aq) ![]() 2AgCl(s)��CrO
2AgCl(s)��CrO![]() (aq)ƽ�ⳣ��K��6.25��107
(aq)ƽ�ⳣ��K��6.25��107
D. ��t ��ʱ����0.001 mol��L��1 AgNO3��Һ�ζ�20 mL 0.001 mol��L��1 KCl��0.001 mol��L��1��K2CrO4�Ļ����Һ��CrO![]() �ȳ���
�ȳ���
���𰸡�D
��������A.��t ��ʱ��Ag2CrO4��KspΪKsp(Ag2CrO4)=c2(Ag+)c(CrO42-)=(1��10��3)2��10��5=1��10��11��A��ȷ��B. �ڱ�����Һ�м���K2CrO4(s)��c(CrO42-)����ʹ��Һ��Y�㵽Z�㣬��B��ȷ��C. ��t ����Ag2CrO4(s)��2Cl��(aq) ![]() 2AgCl(s)��CrO
2AgCl(s)��CrO![]() (aq)��ƽ�ⳣ��K��
(aq)��ƽ�ⳣ��K��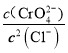 ��
��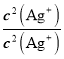 =
=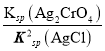 =6.25��107����C��ȷ��D. ��t ��ʱ����ʼ����AgCl����ʱ��c(Ag+)=
=6.25��107����C��ȷ��D. ��t ��ʱ����ʼ����AgCl����ʱ��c(Ag+)=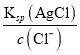 =4��10��7mol/L����ʼ����Ag2CrO4����ʱ��[
=4��10��7mol/L����ʼ����Ag2CrO4����ʱ��[![]() =1��10��4mol/L������Cl-������Ҫ��c(Ag+)��С���ȳ�������D����ѡD��
=1��10��4mol/L������Cl-������Ҫ��c(Ag+)��С���ȳ�������D����ѡD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�̬ԭ�ӻ����ӵĵ����Ų�ʽ������ǣ� ��
A. .Cr��[Ar]3d44s2 B. F-:1s22s22p6
C. K+��1s22s22p63s23p6 D. S��1s22s22p63s23p4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����ϸ������ҪԪ�ؼ������������ͼʾ��Ϣ����������⣺

(1)����ϸ���Ļ���Ԫ����____________��
(2)���������������Ԫ��ռϸ�����ص�________��
(3)________Ԫ����ϸ��������������ռ���������Ҫ����Ϊ______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ����Ⱦ��С���ҿ������������з���δ������Դ�����ǣ� ��
����Ȼ�� ��ú �ۺ��� ��ʯ�� ��̫���� ���������� �߷��� ������
A.�٢ڢۢ�B.�ݢޢߢ�C.�ۢݢޢߢ�D.�ۢܢݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 mol A�����2 mol B���������Ϊ2 L���ܱ������л�ϣ�����һ�������·�����Ӧ��2A(g)��B(g)![]() xC(g)������2s����A�����ʵ���Ϊ2.8 mol��C�����ʵ���Ũ��Ϊ0.6mol/L���������м���˵������2s��������A��ʾ��ƽ����Ӧ����Ϊ0.3 mol/(L��s)����2s��������B��ʾ��ƽ����Ӧ����Ϊ0.6 mol/(L��s)����2sʱ����B��ת����Ϊ70%����x��2��������ȷ����(���� )
xC(g)������2s����A�����ʵ���Ϊ2.8 mol��C�����ʵ���Ũ��Ϊ0.6mol/L���������м���˵������2s��������A��ʾ��ƽ����Ӧ����Ϊ0.3 mol/(L��s)����2s��������B��ʾ��ƽ����Ӧ����Ϊ0.6 mol/(L��s)����2sʱ����B��ת����Ϊ70%����x��2��������ȷ����(���� )
A. �٢� B. �ڢ� C. �٢� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������״��ķϴ���(��Ҫ�ɷ�ΪZnO��CuO,�����������л����ʵ�)��ɢCuCl��ZnO�Ĺ����������£�
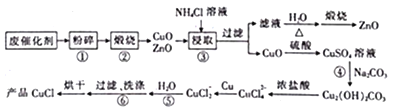
��֪��NH4Cl��Һ��ȡʱ����������Ҫ��Ӧ���£�
ZnO(s)+2NH4Cl(aq)![]() Zn(NH3)2Cl2(aq)+H2O(l)K1=0.042
Zn(NH3)2Cl2(aq)+H2O(l)K1=0.042
CuO(s)+2NH4Cl(aq)![]() Cu(NH3)2Cl2(aq)+H2O(l)K2=0.0065
Cu(NH3)2Cl2(aq)+H2O(l)K2=0.0065
�ش�����ͬ�⣺
(1)Ԥ����ʱ,�ϴ�������С����顱����ҪĿ����________��������С����ա���Ŀ����______________��
(2)����ܷ�����Ӧ�����ӷ���ʽΪ______________________________��
(3)����ݼ�H2Oϡ�͵�Ŀ����____________________________________________��
(4)������ˡ�ϴ��ʱ,��Ҫ�����Ƿ�ϴ�Ӹɾ�����ʵ�������_____________________��
(5)ȷ��ȡmg��ƷCuCl,���������Թ�����FeCl3��Һ�У�����ܽ����������ϡ����,��cmol��L-1��K2Cr2O7��Һ�ζ����յ㣬����K2Cr2O7��Һ�����ΪVmL����֪�ζ�ʱCr2O72-����ԭΪCr3+����ζ������з�����Ӧ�����ӷ���ʽΪ______________________���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ________;�ò�Ʒ��CuCl����������Ϊ________(�ú�c��m��V�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������̼��������ϳɻ���ԭ�ϣ��ȿ��Լ��ٻ�����Ⱦ������ЧӦ�����ܱ��Ϊ����
��CO2���ۺ������ǽ������ЧӦ����Դ�������Ч;����
(1)O2��H2�ڴ��������¿ɷ�����Ӧ����CH3OH����֪CH3OH��H2��ȼ���ȷֱ�Ϊ��H1=-akJ��mol-1����H2=-bkJ��mol-1����1molˮ����ת��ΪҺ̬ˮʱ�ų�ckJ��������
��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)��H=___________kJ��mol-1��
CH3OH(g)+H2O(g)��H=___________kJ��mol-1��
(2)����CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)������CO2��H2��ʼͶ�ϱ�Ϊ1��3ʱ���¶ȶ�CO2ƽ��ת���ʼ��״����ʵ�Ӱ����ͼ��ʾ����ͼ��֪��ȡCH3OH�����˵��¶���___________���������������CO2ת��ΪCH3OH��ƽ��ת���ʵĴ�ʩ��___________��
CH3OH(g)+H2O(g)������CO2��H2��ʼͶ�ϱ�Ϊ1��3ʱ���¶ȶ�CO2ƽ��ת���ʼ��״����ʵ�Ӱ����ͼ��ʾ����ͼ��֪��ȡCH3OH�����˵��¶���___________���������������CO2ת��ΪCH3OH��ƽ��ת���ʵĴ�ʩ��___________��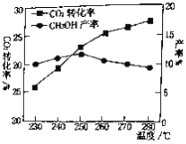
A��ʹ�ô��� B��������ϵѹǿ
C������CO2��H2�ij�ʼͶ�ϱ� D��Ͷ�ϱȲ��������������䣬���ӷ�Ӧ���Ũ��
��CO�Ǻϳ����ء������ԭ�ϡ�
(3)�ϳ����صķ�Ӧ��2NH3(g)+CO(g)![]() CO(NH2)2(g)+H2(g)��H=-81.0kJ��mol-1��
CO(NH2)2(g)+H2(g)��H=-81.0kJ��mol-1��
��T��ʱ�������Ϊ2L�ĺ����ܱ������У���2molNH3��1molCO��Ϸ�����Ӧ��5minʱ��NH3��ת����Ϊ80%����0��5min�ڵ�ƽ����Ӧ����Ϊv(CO)=___________��
����֪��
�¶�/K | 398 | 498 | �� |
ƽ�ⳣ��/K | 126.5 | K1 | �� |
��K1___________126.5(�������<��);���������___________��
(4)ͨ���˹�������ÿɽ�COת����HCOOH��
����֪�����£�Ũ�Ⱦ�Ϊ0.1mol��L-1��HCOOH��HCOONa�����ҺpH=3.7,��HCOOH�ĵ��볣��Ka��ֵΪ___________ (��֪lg2=0.3)��
���õ绯ѧ������HCOOH��ˮ����ɵ���Ⱦ����ԭ���ǵ��CoSO4��ϡ�����HCOOH�����Һ���õ�������Co3+��HCOOH������CO2��Co3+����HCOOH�����ӷ���ʽΪ___________;��������仯�����ǰ��Co2+��Ũ�Ƚ�___________ (�������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������·������з�Ӧ��������������ˮ�ⷴӦ���ǣ� ��
A. Cl2��H2O![]() H����Cl����HClO
H����Cl����HClO
B. HCO3��+ H2O![]() H3O++ CO32��
H3O++ CO32��
C. H2S![]() H����HS��
H����HS��
D. NH4+��2H2O![]() NH3��H2O �� H3O+
NH3��H2O �� H3O+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ����������Һ�У���Ƭ�ܽ⣬��Һ�������ӣ���û������ų����ǣ� ��
A.ϡ����
B.CuSO4��Һ
C.Fe2��SO4��3��Һ
D.AgNO3��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com