
【题目】下列各组反应,前后均可以用同一个离子方程式表示的是
A.HCl+Na2CO3 HCl+NaHCO3
B.HCl+Na2CO3 H2SO4+K2CO3
C.H2S+NaOH H2SO4+KOH
D.BaCl2+Na2SO4 BaCO3+H2SO4
科目:高中化学 来源: 题型:
【题目】氨气在工业上有广泛用途。请回答以下问题:
(1)工业上利用N2(g)+3H2(g) ![]() 2NH3(g) H<0合成氨,某小组为了探究外界条件对该反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图。
2NH3(g) H<0合成氨,某小组为了探究外界条件对该反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图。

①相对a而言,b可能改变的条件是____________,判断的理由是__________________;
②a条件下,0~t0的平均反应速率v(N2)=_____________mol·L-1·min-1;
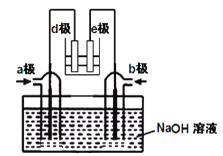
(2)有人利用NH3和NO2构成电池的方法,既能实现有效消除氮氧化物的排放减少环境污染,又能充分利用化学能进行粗铝的精炼,如图B所示,e极为精铝。
a极通入____气体(填化学式),判断的理由是___________________________________;
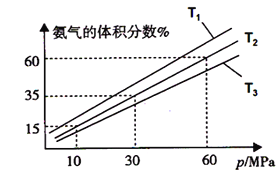
(3)某小组往一恒温恒压容器充入9mol N2和23mol H2模拟合成氨反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。
①能判断N2(g)+3H2(g) ![]() 2NH3(g)达到平衡的是______(填序号) ;
2NH3(g)达到平衡的是______(填序号) ;
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(N2)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②若T1、T2、T3温度下的平衡常数分别为K1、K2、K3,则K1、K2、K3由大到小的排序为_______________,
③此时N2的平衡分压为__________Mpa,(分压=总压×物质的量分数)
计算出此时的平衡常数Kp=________。(用平衡分压代替平衡浓度计算,结果保留2位有效数字并带上单位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种有机物中:A.CH4;B.CH2=CH2;C.CH3CH2OH;D.CH3COOH;E.淀粉。
(1)C分子中含有的官能团的名称是_____;
(2)A分子的结构式是_____;
(3)水溶液显酸性的是_____(填编号);
(4)可用于合成聚乙烯塑料的是_____(填编号),化学反应方程式为_____________________ ;
(5)通常用于检验碘单质的是_____(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.短周期元素X、Y、Z、R在周期表中的相对位置如图所示,请回答以下问题:

(1)X的原子结构示意图为________,其在周期表中的位置为_______________。
(2)Y与Z的原子半径大小关系是:Y____Z (填“>”或“<”)。
(3)X与R的非金属性强弱顺序是:X____R (填“>”或“<”)。
(4)位于Y下一周期的同主族元素的最高价氧化物对应的水化物的化学式为______。
II.研究表明,在高压与加热的条件下,钠、氦、氧三种元素能形成一种结构特殊的固态化合物Na2HeO。
(1)化合物Na2HeO中氦元素的化合价为0,其中氧元素的化合价为______。
(2)钠、氦气、氧气反应生成Na2HeO的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰及其化合物在生产、生活中有许多用途。在实验室中模拟工业利用软锰矿(主要成分为MnO2,含少量SiO2、Fe2O3和Al2O3等)制备金属锰等物质,设计流程如下:

己知:Mn2+有较强的还原性,在空气中能被氧气氧化,碳酸锰在空气中高温加热固体产物为Mn2O3;部分氢氧化物的Ksp(近似值)如下表。
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
(1)“酸浸”前需将软锰矿粉碎的目的是_____________;酸浸过程MnO2发生反应的离子方程式为_________________。
(2)向滤液I中需先加A物质,再加B物质,若加入的物质均为非金属化合物的溶液,则A为(填物质的名称)_________,B为(填物质的名称)________。滤渣II的成分是_______(填物质的化学式)。
(3)“酸浸”需适宜的酸浓度、液固比、酸浸温度等,其中浸取率随酸浸时间的变化如图所示:

当浸取时间超过4h时,锰浸取率反而减小,其原因是______________。
(4)测得滤液I中c(Mn2+)=0.1mo/L,则加入B调节溶液pH范围为______。(已知:当某种离子浓度小于1×10-5mo/L时,可认为其沉淀完全。结果保留两位小数)
(5)“沉锰”过程中加入氨水的目的是(从化学平衡移动的角度解释)______________。
(6)写出由MnCO3为原料制备金属锰的过程中所涉及的化学方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com