
����Ŀ����һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ(��֪��Ӧ���̷���)���������������ֺ���Ԫ�ص����ӣ�����ClO����ClO3���������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ����ͼ��ʾ������˵����ȷ���ǣ� ��
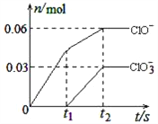
A. ���Լ���Һ��KOH�����ʵ�����0.09mol
B. ClO3�����������������������Ķ��������
C. ������������ClO����ClO3��������Cl2
D. ��Ӧ��ת�Ƶ��ӵ����ʵ�����0.21mol
���𰸡�D
�����������������A������������������Һ��Ӧ���ɴ�����ء��Ȼ��غ�����أ�����ͼ��֪n��ClO-��=0.06mol��n��ClO3-��=0.03mol�����ݵ���ת���غ��֪���ɵ�������n��Cl-��=0.06mol����1-0��+0.03mol����5-0��=0.21mol�����������غ��֪n��K+��=n��Cl-��+n��ClO-��+n��ClO3-��=0.21mol+0.06mol+0.03mol=0.3mol�����������ص����ʵ���=0.3mol��A����B����0��t1��û��ClO3�������ɣ�˵�����¶��йأ�B����C��ClO����ClO3�������ܿ�����Cl2����Ϊ�����ܶ��õ��ӣ�C����D����Ӧ��ת�Ƶ��ӵ����ʵ�����0.21mol��D��ȷ����ѡD


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������100ml1.0mol/LNa2SO4��Һ����ȷ�ķ�����
�ٽ�14.2gNa2SO4����100mlˮ��
�ڽ�32.2gNa2SO4��10H2O��������ˮ�У�����ˮϡ����100mL
�۽�20mL5.0 mol/LNa2SO4��Һ��ˮϡ����100mL
A. �٢� B. �٢ڢ� C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����T��ʱ,������ӦC(s)+H2O(g) ![]() CO(g)+H2(g)��
CO(g)+H2(g)��
��1��T��ʱ,��һ��2L���ܱ������м���4molC��1molH2O(g),5min��Ӧ�ﵽƽ��,C��ת����Ϊ20%��
��0��5min��,��H2O(g)��ʾ��ƽ����Ӧ����Ϊ____________��
�ڸ÷�Ӧ�ﵽƽ��ı�־��______��
a.�����ƽ����Է�����������
b.������ܶȲ���
c.H2O(g)��CO(g)��H2(g)�����ʵ���֮��Ϊ1��1:1
d.����������ʵ�������
��2��T��ʱ,�������ܱ������м�����Ӧ�����ʽ���ʵ��,�м�ĸ���������ɻ�����

���������������ƽ����Է�������һֱ���ֲ��䣬��Ӧ��ʼǰH2O(g)��H2(g)�����ʵ���֮����__________��
�ڷ�Ӧ�ڴﵽƽ��ʱ,�м�ĸ���������λ����________��
a.1��1.5֮�� b.1.5�� c.1.5��2֮��
��3����֪:I.�ƻ�1mol���ۼ�����Ҫ���������±���
���ۼ� | ʯī�е�̼̼�� | H-H | C��O | H-O |
����/kJ | 475.7 | 436 | 1072 | 463 |
��.ʯī���������η䳲�ṹ��̼ԭ�ӹ��ɣ���ͼ��ʾ:
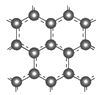
ijͬѧ����:ͨ������װ��ʵ��C(s)+H2O(g) ![]() CO(g)+H2(g)�ķ�Ӧ��
CO(g)+H2(g)�ķ�Ӧ��
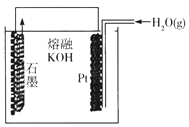
�ٰ��ÿ����Ĺ���,ʯī�缫�����ķ�ӦʽΪ_______________��
��������������?˵������: _______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������в���ȷ����
A. ����Ũ�ȵĴ�������Һ��ʹ��̪��Һ��죬��ԭ���Ƿ��������·�Ӧ��CH3COO-+H2O![]() CH3COOH +OH-��ʹ����Һ�е�c(OH-)>c(H+)
CH3COOH +OH-��ʹ����Һ�е�c(OH-)>c(H+)
B. �ڳ����£�10mL0.02 mol/L��������10mL0.02 mol/LBa(OH)2��Һ��ֻ�ϣ�����Ϻ���Һ�����Ϊ20 mL������Һ��pH=12
C. ��0.1mol/L NH4Cl��Һ�У�c(H+)+c(NH4+) = n(Cl-)+c(OH-)
D. 5mL 1mol/LCH3COONa��Һ��5 mL1mol/L �����Ϻ��Һ�У�c(Cl-)>c(Na+)>c(H+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ�в�����Al3+ ���������������
A. Cl- B. OH- C. H+ D. Na+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ����ѧ���̵�ʾ��ͼ���ش��������⣺ 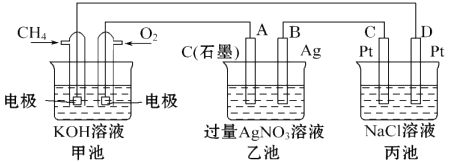
��1����װ����ͨ��CH4�ĵ缫��ӦʽΪ ��
��2��������ת���ĽǶȷ������ҳ���ת��Ϊ��װ�ã�
��3��һ��ʱ�䣬�������в���112mL����״���£�����ʱ�����Ƚ�����أ�������Һ��25��ʱ�����ʵ���Ũ��Ϊ �� ����֪��NaCl��Һ������������Һ���Ϊ500mL����
��4����Ҫʹ���ػָ����ǰ��״̬��Ӧ�������ͨ����д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ(Ӳ֬����)�ֱ�װ����֧�Թ��У�����һ֧�Թ��м���ϡ���������������ڶ�֧�Թ��м���MgCl2��Һ����������д����֧�Թ��з�Ӧ�ķ���ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ���Ͱ���Ϊͬ�������� B. CH3CH2OH��CH3OCH3��Ϊͬ���칹��
C. 12C��14C��Ϊͬλ�� D. ����21H��������Ϊ0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ��ˮ���ܼ����һ��������( )
A.�������ᡢ���Ȼ�̼
B.�Ҵ�����ȩ������
C.��ȩ���Ҷ�����������
D.���ӡ��Ҵ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com