
分析 弱酸是指水溶液中部分电离的酸,强酸是水溶液中全部电离的酸,
弱碱是指水溶液中部分电离的碱,强碱是水溶液中全部电离的碱,
正盐是酸碱恰好完全中和生成的盐,
酸式盐是多元酸和碱部分反应生成的盐,碱式盐是指多元碱和酸部分反应生成的盐,
酸性氧化物是指和碱反应生成盐和水的氧化物,碱性氧化物是和酸反应生成盐和水的氧化物,
离子化合物是阴阳离子通过静电作用形成的化合物,共价化合物是仅有共价键形成的化合物,
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,可以是金属置换金属,金属置换非金属,非金属置换非金属,非金属置换金属等.
解答 解:由H、O、Cl、C、Cu、Na、S、N中的元素组成的化合物,
弱酸:HClO、H2CO3、H2SO3、H2S、HNO2,强酸:HCl、HClO4、H2SO4、HNO3,
强碱:NaOH,弱碱:Cu(OH)2、NH3•H2O,
正盐:CuCl2、CuCO3、CuS、CuSO3、CuSO4、Cu(NO3)2、Cu(NO2)2,NaCl、Na2CO3、Na2S、Na2SO3、Na2SO4、NaNO3、NaNO2,
酸式盐:NaHS、NaHSO3、NaHSO4、NaHCO3,碱式盐:Cu2(OH)2CO3,
酸性氧化物:Cl2O7、CO2、SO2、SO3、N2O3、N2O5,碱性氧化物:Na2O、CuO,
离子化合物:CuCl2、CuCO3、CuS、CuSO3、CuSO4、Cu(NO3)2、Cu(NO2)2,NaCl、Na2CO3、Na2S、Na2SO3、Na2SO4、NaNO3、NaNO2、NaHS、NaHSO3、NaHSO4、NaHCO3、Na2O、CuO、NaOH、Cu(OH)2,
共价化合物:HClO、H2CO3、H2SO3、H2S、HNO2、HCl、HClO4、H2SO4、HNO3、Cl2O7、CO2、SO2、SO3、N2O3、N2O5,
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,可以是金属置换金属,金属置换非金属,非金属置换非金属,非金属置换金属,
故答案为:HClO、H2CO3、H2SO3、H2S、HNO2;HCl、HClO4、H2SO4、HNO3;
NaOH;Cu(OH)2、NH3•H2O;
CuCl2、CuCO3、CuS、CuSO3、CuSO4、Cu(NO3)2、Cu(NO2)2;NaCl、Na2CO3、Na2S、Na2SO3、Na2SO4、NaNO3、NaNO2;
NaHS、NaHSO3、NaHSO4、NaHCO3;Cu2(OH)2CO3;
Cl2O7、CO2、SO2、SO3、N2O3、N2O5;Na2O、CuO;
CuCl2、CuCO3、CuS、CuSO3、CuSO4、Cu(NO3)2、Cu(NO2)2;NaCl、Na2CO3、Na2S、Na2SO3、Na2SO4、NaNO3、NaNO2、NaHS、NaHSO3、NaHSO4、NaHCO3、Na2O、CuO、NaOH、Cu(OH)2;
HClO、H2CO3、H2SO3、H2S、HNO2、HCl、HClO4、H2SO4、HNO3、Cl2O7、CO2、SO2、SO3、N2O3、N2O5;
置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,可以是金属置换金属,金属置换非金属,非金属置换非金属,非金属置换金属.
点评 本题考查了物质分类、物质组成、物质结构特征和化学式的书写等,掌握是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C5H6O | B. | C5H12 | C. | C5H12O2 | D. | C5H12O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是在法国拍卖会拍卖的我国圆明园兽首--兔首和鼠首,拍卖台上渴望回家的铜器兔首和鼠首看上去仍熠熠生辉.下列对其原因的分析,最可能的是( )
如图是在法国拍卖会拍卖的我国圆明园兽首--兔首和鼠首,拍卖台上渴望回家的铜器兔首和鼠首看上去仍熠熠生辉.下列对其原因的分析,最可能的是( )| A. | 它们的表面都电镀上了一层耐腐蚀的黄金 | |
| B. | 环境污染日趋严重,它们表面的铜绿被酸雨溶液洗去 | |
| C. | 铜的活动性比氢弱,因此不易被氧化 | |
| D. | 它们是含一定比例金、银、锡、锌的铜合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机高分子化合物的合成对提高人类的生活质量有重要的作用 | |
| B. | 依赖化学反应生产的化学肥料在农业生产中的使用对解决人类的吃饭问题贡献突出 | |
| C. | 化学越发展,环境污染越严重 | |
| D. | 海水、矿物的综合利用大多依赖于化学方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1000a}{98ρ}$×100% | B. | $\frac{98ρ}{1000a}$×100% | C. | $\frac{1000ρ}{98a}$×100% | D. | $\frac{98a}{1000ρ}$×100% |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学卷(解析版) 题型:选择题
实验室用足量锌粉与一定量的某浓度的盐酸反应来制氢气。为便于收集气体欲减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
A.K2SO4固体 B.NaOH溶液 C.少量CuSO4溶液 D.CH3COONa固体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高一上10月月考化学卷(解析版) 题型:选择题
下列说法正确的是
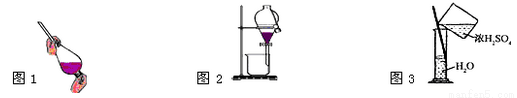
A. 萃取操作时,振荡过程中需要放气,放气是通过打开分液漏斗上口的玻璃塞进行的
B. 可以采用蒸发浓缩、冷却结晶的方法从硝酸钾溶液中获得硝酸钾晶体
C. 将乙醇与水分离,如图1、图2操作
D. 稀释浓H2SO4,如图3操作
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com