
【题目】已知浓硫酸与乙醇的混合液加热后可产生乙烯。为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:将生成的气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应。
乙同学在甲同学的实验中,发现褪色后的溶液中有硫酸根离子,推测在制得的乙烯中还可能有少量还原性气体杂质,由此他提出必须先除去,再与溴水反应。
请回答下列问题:
(1)甲同学实验中溴水褪色的主要的化学方程式为______________________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴水发生加成反应,理由是________。
a.使溴水褪色的反应未必是加成反应
b.使溴水褪色的反应就是加成反应
c.使溴水褪色的物质未必是乙烯
d.使溴水褪色的物质就是乙烯
(3)乙同学推测乙烯中必定含有的一种气体是________,可以用________来验证,这种气体与溴水反应的化学方程式是_____________________________________________。
(4)为验证溴水褪色的反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性的方法,理由是________________________________________________。
【答案】CH2===CH2+Br2―→CH2BrCH2Br 不能 ac SO2 品红溶液 2H2O+Br2+SO2===2HBr+H2SO4 如发生取代反应,必定生成HBr,溶液酸性将明显增强,故可用pH试纸验证
【解析】
这是一道有机实验题,考查学生整体分析问题的能力,从题给材料知乙烯与溴水发生加成反应,即:CH2===CH2+Br2―→![]() 。乙同学发现甲同学实验中褪色后的溶液中有SO42—,可推知乙烯气体中含有还原性气体,含有S元素可能是SO2,结合制取C2H4的原料是浓H2SO4与乙醇,可推知浓H2SO4使部分乙醇脱水碳化,在加热时,碳与浓H2SO4发生氧化还原反应生成SO2气体,到这里问题便迎刃而解。
。乙同学发现甲同学实验中褪色后的溶液中有SO42—,可推知乙烯气体中含有还原性气体,含有S元素可能是SO2,结合制取C2H4的原料是浓H2SO4与乙醇,可推知浓H2SO4使部分乙醇脱水碳化,在加热时,碳与浓H2SO4发生氧化还原反应生成SO2气体,到这里问题便迎刃而解。
(1)乙烯中含碳碳双键,可与溴水发生加成反应生成1,2-二溴乙烷,方程式为:CH2═CH2+Br2→CH2Br-CH2Br,故答案为:CH2═CH2+Br2→CH2Br-CH2Br;
(2)用此法得到的乙烯内可能含有SO2气体,因SO2能将溴水还原而使之褪色,方程式为:SO2+Br2+2H2O═2HBr+H2SO4,溴水褪色不能证明是乙烯与溴水发生了加成反应,故答案为:不能;ac;
(3)乙烯中可能含有的一种杂质气体是SO2,二氧化硫可以用品红溶液检验,二氧化硫能使品红溶液褪色,加热恢复红色,它与溴水发生反应的化学方程式是SO2+Br2+2H2O═2HBr+H2SO4,故答案为:品红溶液;SO2+Br2+2H2O═2HBr+H2SO4;
(4)加成反应无HBr生成,而取代反应则有HBr生成,若乙烯和溴发生取代反应,则该反应中有溴化氢生成,用pH试纸测反应后溶液应该呈酸性,如果溶液没有呈酸性,则证明发生加成反应,故答案为:如发生取代反应,必定生成HBr,溶液酸性将明显增强,故可用pH试纸验。


科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理锂电池废料以节约资源、保护环境。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示:
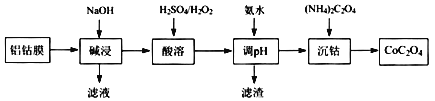
回答下列问题:
(l) Li元素在元素周期表中的位置为____________,LiCoO2中Co的化合价是____。
(2)“碱浸”时Al溶解的离子方程式为________。
(3)“酸溶”时加入H2O2的目的是____,调节pH后所得滤渣主要为____。
(4)“沉钴”的离子方程式为________。
(5)配制100 mL l.0 mol/L (NH4)2C2O4溶液,需要的玻璃仪器除玻璃棒、烧杯外,还需要_________。
(6)取CoC2O4固体4.41 g在空气中加热至300℃,得到钴的氧化物2.41 g,则该反应的化学方程式为 _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、W 均为周期表中前四周期的元素,其原子序数依次增大;X2-和 Y+有相 同的核外电子排布;Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R 的基 态原子在前四周期元素的基态原子中单电子数最多;W 为金属元素,X 与 W 形成的某 种化合物与 Z 的氢化物的浓溶液加热时反应可用于实验室制取 Z 的气态单质。回答下 列问题(相关回答均用元素符号表示):
(1)R 的基态原子的核外电子排布式是__________________。
(2)Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是______________。
(3)X 与 Z 中电负性较大的是_____ 。Z 的某种含氧酸盐常用于实验室中 X 的单质的 制取,此酸根离子的空间构型是______________,此离子中含有的化学键类型 是_________ ,X—Z—X 的键角_______109.5°(填“>”、“=”或“<”)。
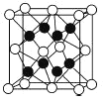
(4)X 与 Y 形成的化合物 Y2X 的晶胞如图。其中 X 离子的配位数 为___________,以相距一个 X 离子最近的所有 Y 离子为顶点构成的几何体为___________ 。该化合物与 MgO 相比,熔点较高的是____________。
(5)已知该化合物的晶胞边长为 a pm,则该化合物的密度为________________g·cm-3(只要求列算式,不必计算出数值,阿伏加德岁常数的数值为 NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】思维辨析:
(1)乙醇易溶于水,是因为乙醇分子间存在氢键。________
(2)HO—CH2CH2—OH也可与Na反应,断裂C—O键。________
(3)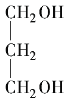 的命名是1,3二丙醇。________
的命名是1,3二丙醇。________
(4)1丙醇在氢氧化钠溶液中加热也可发生消去反应。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将29.5 g乙烷和乙烯组成的混合气体缓缓通入足量的溴水后,溴水增重7 g。则原混合气体中,乙烯的体积分数为
A.76%B.50%C.30%D.25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是( )
A. 1 molCH3COOH与1mol CH3CH2OH在浓硫酸共热下生成的乙酸乙酯分子数为NA
B. 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
C. 7.8g ![]() 中含有的碳碳双键数为0.3NA
中含有的碳碳双键数为0.3NA
D. 标准状况下,11.2L的戊烷所含的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g);△H=a kJ/mol,下列叙述不正确的是( )

A. 反应过程中能量关系如上图表示,则该反应为放热反应
B. 若将该反应设计成原电池,锌为负极
C. 化学反应的焓变与反应方程式的计量数有关
D. 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物丙可由如图反应得到,则丙的结构不可能是
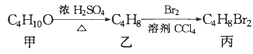
A. CH3CBr2CH2CH3B. (CH3)CBrCH2Br
C. CH3CH2CHBrCH2BrD. CH3(CHBr)2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g);ΔH=+QkJ·mol-1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
Si(s)+4HCl(g);ΔH=+QkJ·mol-1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C.反应至4min时,若HCl浓度为0.12mol·L-1,则H2反应速率为0.03mol·L-1·min-1
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH溶液恰好反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com