
【题目】北京奥运会主体育场“鸟巢”,被《泰晤士报》评为全球“最强悍”工程。“鸟巢”运用了高强度、高性能的钒氮合金高新钢,则钒原子的价电子排布式正确的是( )
A. 3s23p6B. 3d34s2C. 3d64s2D. 4s2
科目:高中化学 来源: 题型:
【题目】全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:VO2+(蓝色)+H2O+V3+(紫色)![]() VO2+(黄色)+V2+(绿色)+2H+ 下列说法错误的( )
VO2+(黄色)+V2+(绿色)+2H+ 下列说法错误的( )
A. 充电时,反应每生成2molH+时电子转移的物质的量为2mol
B. 放电过程中,正极附近溶液的酸性减弱
C. 放电时,正极反应为VO2++2H++e-=VO2++H2O
D. 充电时,阳极附近溶液由蓝色逐渐变为黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是 ( )
A. 放热反应在常温下不一定能直接发生
B. 需要加热方能发生的反应一定是吸热反应
C. 反应是放热还是吸热须看反应物和生成物具有的总能量的相对大小
D. 吸热反应在一定条件下也能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品工业和食品工业,下图是乙酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。已知A是果实的催熟剂。

(1)A分子的电子式为________;C的分子式为________;D中官能团结构简式为________。
(2)A→B反应类型为_____________,反应F→G反应类型___________。
(3)G的同分异构体有多种,遇FeCl3溶液显紫色的共有_____种;
苯环上一氯代物有2种的物质的结构简式______________。
(4)写出下列反应的化学方程式:
B→C:_____________________;
F→G:______________________;
G→H:___________________;
C的银镜反应方程式为:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CH4是两种温室气体,研究它们具有重要的意义。
(1)已知CH4、H2和CO的燃烧热(△H)分别为-890.3 kJ· mol-1、-285.8 kJ· mol-1和-283.0 kJ·mol-1。则![]()
![]() △H=_________kJ·mol-1
△H=_________kJ·mol-1
(2)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示为: ![]()
![]() △H=-86.98 kJ·mol-1
△H=-86.98 kJ·mol-1
反应中影响CO2平衡转化率的因素很多,右图为某特定条件下,不同水碳比[n(H2O/n(CO2)]和温度对CO2平衡转化率的影响曲线。

①为提高CO2的平衡转化率,生产中除控制温度外还可以采取的措施有___________________、____________________。
②当温度高于190℃后,CO2平衡转化率出现如图所示的变化趋势,其原因是_______________。
(3)向1.0 L密闭容器中通入0.2 mol NH3(g)和0.1 mol CO2(g),在一定温度下发生反应则![]()
![]() ,反应时间与气体总压强(p)的数据如下表:
,反应时间与气体总压强(p)的数据如下表:
![]() 用起始压强和总压强计算平衡时NH3的转化率为_________,0~80 min内CO2的平均反应速率是__________。
用起始压强和总压强计算平衡时NH3的转化率为_________,0~80 min内CO2的平均反应速率是__________。
(4)氨基甲酸铵(NH2COONH4)极易水解成碳酸铵,在酸性条件水解更彻底。将氨基甲酸铵粉末逐渐加入到1 L 0.1 mol·L-1的盐酸中直到pH=7(室温下,忽略溶液体积变化),共用去0.052 mol氨基甲酸铵,溶液中几乎不含碳元素。此时溶液中c(NH4+)=__________,NH4+水解平衡常数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2C12是橡胶工业上常用的硫化剂,是一种金黄色液体。
已知:①S2C12不稳定,进一步氯化可得SCl2;②S2Cl2、SCl2都能与水反应, ![]() ==
== ![]() ==
==![]() ;③几种物质的熔沸点如表:
;③几种物质的熔沸点如表:

下图是实验室中通过向熔融的单质硫中通入少量氯气制取S2Cl2的装置(部分夹持、加热装置已略去)。

(1)B装置中仪器a的名称___________。
(2)装置的连接顺序是(每个装置只能使用一次)________________________________。
(3)装置D的作用是_________。
(4)实验开始时先点燃_______酒精灯再点燃 _______处酒精灯。
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是_________,该操作的温度范围是___________。
(6)请设计实验证明所得产品中是否含有杂质SCl2_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. lmol苯乙烯中含碳碳双键数为4NA
B. 28g聚乙烯中含有的碳原子数目为2NA
C. 5.6g乙烯和环丁烷(C4H8)的混合气体完全燃烧需O2为1.2NA
D. 标准状况下,11.2L甲醇中含有的分子数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是( )
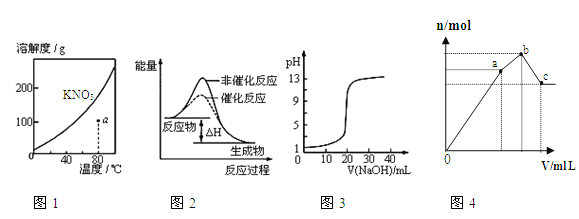
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000molL-1NaOH溶液滴定20.00mL0.1000molL-1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com