
����Ŀ����1����0.2mol/L HA ��Һ�� 0.1mol/L NaOH��Һ�������ϣ���û����Һ��c��Na+��>c��A������������>������<������=����д���пհ�����
�������Һ��c��A��_________c��HA����
�������Һ��c��HA�� + c��A�� 0.1mol/L��
��2������ʱ��ȡ0.1molL-1 HX��Һ��0.1molL-1 NaOH��Һ������������Ϻ���Һ����ı仯��������û����Һ��pH=8���Իش��������⣺
�������Һ����ˮ�������c��OH-����0.1molL-1 NaOH��Һ����ˮ�������c��OH-��֮��Ϊ ��
����֪NH4X��Һ�����ԣ���֪��HX��Һ���뵽Na2CO3��Һ��������ų������ƶ���NH4��2CO3��Һ��pH__________7��ѡ����������������������������
���𰸡�
��1��������������
��2����107��1��107��������
��������
�����������1������0.2mol/L HA ��Һ�� 0.2mol/L NaOH��Һ�������ϣ�����Һ�е�������NaA�����ʵ���Ũ����0.1mol/L�������Һ��c��Na+����c��A-����˵��A-����ˮ���Լ��ԣ�A-+H2O![]() HA+OH-��c��HA����c��A-�����ʴ�Ϊ������
HA+OH-��c��HA����c��A-�����ʴ�Ϊ������
����Һ��c��H+����c��OH-������ҺNaA�ʼ��ԣ����������غ��c��HA��+c��A-��=0.1mol/L���ʴ�Ϊ��=��
��2������ʱ��ȡ0.1molL-1HX��Һ��0.1molL-1 NaOH��Һ������������Ϻ���Һ����ı仯���������������ʵ�����ȣ�����ǡ�÷�Ӧ����NaX����û����Һ��pH=8�������Һ�ʼ��ԣ�˵��NaX��ǿ�������Σ���HX�����
�������Һ����ˮ�������c��OH-��=![]() mol/L=10-6mol/L��0.1mol/LNaOH��Һ����ˮ�������c��OH-��=
mol/L=10-6mol/L��0.1mol/LNaOH��Һ����ˮ�������c��OH-��=![]() mol/L=10-13mol/L�������Һ����ˮ�������c��OH-����0.1molL-1NaOH��Һ����ˮ�������c��OH-��֮��=10-6mol/L��10-13mol/L=107��1���ʴ�Ϊ��107��1��
mol/L=10-13mol/L�������Һ����ˮ�������c��OH-����0.1molL-1NaOH��Һ����ˮ�������c��OH-��֮��=10-6mol/L��10-13mol/L=107��1���ʴ�Ϊ��107��1��
��NH4X��Һ�����ԣ�˵��NH4+��X-����ˮ��̶���ȣ���һˮ�ϰ���HX����ƽ�ⳣ����ȣ�HX��Һ���뵽Na2CO3��Һ��������ų���˵��HX���Դ���H2CO3����CO32-ˮ��̶ȴ���NH4+�����Ը���Һ�ʼ��ԣ�pH��7���ʴ�Ϊ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̶��ݻ�Ϊ2L���ܱ������з�����ӦxA��g��+yB��g��![]() zC��g����ͼI��ʾt��ʱ�����и����ʵ�����ʱ��ı仯��ϵ��ͼII��ʾƽ�ⳣ��K���¶ȱ仯�Ĺ�ϵ�����ͼ���жϣ����н�����ȷ������ ��
zC��g����ͼI��ʾt��ʱ�����и����ʵ�����ʱ��ı仯��ϵ��ͼII��ʾƽ�ⳣ��K���¶ȱ仯�Ĺ�ϵ�����ͼ���жϣ����н�����ȷ������ ��
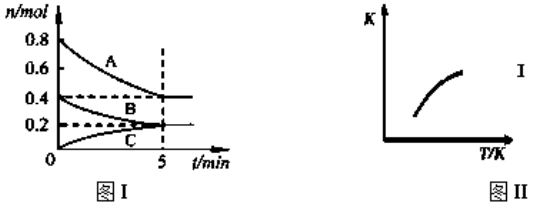
A���÷�Ӧ�ɱ�ʾΪ��2A��g��+B��g��![]() C��g�� ��H��0
C��g�� ��H��0
B��t��ʱ�÷�Ӧ��ƽ�ⳣ��K=6.25
C���������������ܶȲ��ٱ仯ʱ���÷�Ӧ�ﵽƽ��״̬
D��t�����ڵ�6 minʱ������ϵ�г���0.4 mol C���ٴδﵽƽ��ʱC�������������0.25
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ�����ܴﵽʵ��Ŀ����
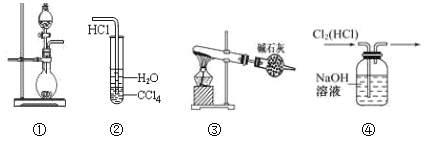
A. ͼ����������ȡ����NH3����MnO2��Ũ������ȡCl2
B. װ�����������Ȼ�����������ˮ
C. ��NH4ClΪԭ�ϣ�װ����������ʵ�����Ʊ����������NH3
D. װ���������ڳ�ȥCl2�е�HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ת����ϵ�ж�����˵����ȷ����(��Ӧ��������ȥ)

A. ��Ӧ�٢ڢۢܢݾ�����������Ӧ�����ӷ�Ӧ
B����Ӧ��˵�������������Ļ�ԭ��ǿ����
C����ͬ���������ɵ�����O2����Ӧ�ۺ͢�ת�Ƶĵ�����֮��Ϊ1��1
D����Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25����101kPa�³��ȼ��һ��������(C4H10)����ų�������ΪQ kJ����5mol/L��KOH��Һ100mL��ȫ�������ɵ�CO2������֮�������Σ������ȼ���ȵ���ֵ��
A��16Q B��8Q C��4Q D��2Q
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH=1����ɫ��Һ�У����������ܴ����������
A��NH4+��Ba2+��NO3- ��CO32- B��Fe2+��OH-��SO42-��MnO4-
C��Na+��Fe3+��Cl-��AlO2- D��K+��Mg2+��NO3-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�һ�ַ�Ӧ���������һ�ַ�Ӧ���Բ�����ȫ��Ӧ������ ��
A. �����������뵪�� B. ������Ũ�������������
C. ������Ũ������ͭ D. ������п��18mol/L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������������ȷ����
A��64 g SO2������ԭ����Ϊ1NA
B�����ʵ���Ũ��Ϊ0.5 mol��L��1��MgCl2��Һ������Cl����Ϊ1 NA
C����״���£�22.4 L H2O�ķ�����Ϊ1NA
D�����³�ѹ�£�14 g N2���з�����Ϊ0.5 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2�Ǹ�Ч������������Ʊ���Ӧ2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4���÷�Ӧ��
A. ClԪ�ر����� B. H2SO4��������
C. SO2�ǻ�ԭ�� D. NaClO3�ǻ�ԭ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com