
【题目】向盛有50 mL 1.00 mol·L1 盐酸的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列说法不正确的是

A.该实验表明化学能可以转化为热能
B.NaOH溶液的浓度大于1.00 mol·L1
C.V=50 mL时,混合溶液的pH>7
D.该实验表明有水生成的反应都是放热反应
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
A. 简单离子半径:W<X<Z B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的叙述中不正确的是( )
A. 第ⅡA族中无非金属元素
B. 第ⅠA族金属元素单质均能与水反应
C. 元素种类最多的族是第Ⅷ族
D. 金属元素的种类比非金属元素多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热化学方程式:C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=+131.3 kJ/mol
CO(g)+H2(g) ΔH=+131.3 kJ/mol
H(g)+ H(g)![]() H2(g) ΔH=435.7 kJ/mol
H2(g) ΔH=435.7 kJ/mol
下列说法正确的是
A.氢原子的能量比氢分子的能量低
B.2个氢原子结合生成1个氢分子,放出435.7 kJ的能量
C.1 mol固态碳与1 mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3 kJ
D.固态碳与液态水反应生成一氧化碳气体和氢气吸收131.3 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R元素的原子有三个电子层,M层电子数是K层电子数的3倍,对R元素的判断不正确的是 ( )
A. R元素处于第三周期ⅥA族 B. R元素是非金属元素
C. 原子核外共有14个电子 D. R元素最低化合价为-2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是:( )
A. c(NH4+)=c(SO42-) B. c(NH4+)>c(SO42-)
C. c(NH4+)<c(SO42-) D. c(OH-)+c(SO42-) = c(NH4+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用质量分数为98%的浓硫酸(ρ=1.84 g·cm-3)配制240 mL 1.84 mol·L-1稀硫酸,下列操作正确的是( )
A. 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B. 必需的定量仪器有100 mL量筒、250 mL容量瓶和托盘天平
C. 量取浓硫酸的体积为25.0 mL
D. 先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如下图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
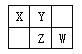
请回答下列问题:
(1)元素Z位于周期表中的位置_____________________。
(2)X、Y、Z三种元素的最高价氧化对应水化物中酸性由强到弱依次为________________(写化学式)。
(3)X和Y形成一种有毒的二元化合物,其相对分子质量在50~60之间,且其分子式中X的质量分数约为46%,该化合物的分子式为__________,该分子中各原子最外层均满足8电子稳定结构,其结构式为 ___________.
(4)写出W的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式_____________,
反应中若转移12mol电子,消耗的还原剂质量为______g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com