
ij�¶��£���һ��������ܱ�������X��Y��Z��W��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±�
 ������˵��������� �� ��
������˵��������� �� ��
���� | X | Y | Z | W |
��ʼŨ��/mol��L-1 | 0.5 | 0.6 | 0 | 0 |
ƽ��Ũ��/mol��L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
 A������ѹǿ��Ӧ��ƽ�ⳣ�����䣬��X��ת��������
A������ѹǿ��Ӧ��ƽ�ⳣ�����䣬��X��ת��������
 B���÷�Ӧ�Ļ�ѧ����ʽΪ��4X (g)��5Y (g)
B���÷�Ӧ�Ļ�ѧ����ʽΪ��4X (g)��5Y (g) 4Z (g)+ 6W (g)
4Z (g)+ 6W (g)
 C����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ80%
C����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ80%
 D�������������䣬������Y����ʼŨ�ȣ�X��ת��������
D�������������䣬������Y����ʼŨ�ȣ�X��ת��������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭��Ҧ��ѧ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��Һ���������Һ�����ַ�ɢϵ�ĸ���������
A���Ƿ��Ǵ������ӻ����ӵļ�����
B���Ƿ���ͨ����ֽ
C����ɢ������ֱ���Ĵ�С
D���Ƿ��һ�������ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�������һ��ѧ����һ���չٿ���һ���ۻ�ѧ���������棩 ���ͣ������
��������ϡ�������ij��ʯ�����Һ�У����˺��д��������⣮����������NH4+��Fe3+��AsO43-��Cl-��Ϊ��ȥ�������ӣ����ֲ����������£�
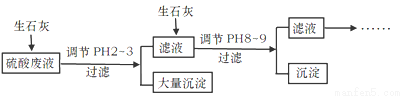
��ش����⣺
��1��NH4+����ϡ�������ij��ʯ�����Һ����(NH4)2SO4��NH4Cl��ʽ���ڣ�����һ��(NH4)2SO4��Һ��һ��NH4Cl��Һ��(NH4)2SO4��Һ��c(NH4+)ǡ����NH4Cl��Һ��c(NH4+)��2������c[(NH4)2SO4]_____c(NH4Cl)(�<��= �� >) ��
��2���������Һ��Ͷ����ʯ�ң�������Һ�¶ȵı仯������Һ��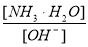 ______(���������С�����䡱)��
______(���������С�����䡱)��
��3��Ͷ����ʯ�ҵ���pH��2��3ʱ������������Ҫ�ɷ�ΪCaSO4��2H2O[��������Fe(OH)3]���ᴿCaSO4��2H2O����Ҫ���裺������м������_______����ַ�Ӧ���ˡ�ϴ�ӡ�______��
��4��25�棬H3AsO4���볣��ΪK1=5.6��10-3��K2=1.7��10-7��K3=4.0��10-12������Һ��pH���ڵ�8��9ʱ��������Ҫ�ɷ�ΪCa3(AsO4)2.
��pH���ڵ�8����Ca3(AsO4)2 �ſ�ʼ������ԭ����________��
�� Na3AsO4 ��һ��ˮ���ƽ�ⳣ����ֵΪ��________��
����֪��AsO43-+2I-+2H+= AsO43-+I2+H2O��SO2+I2+2H2O=SO42-+2I-+4H+ ������������Ӧ�л�ԭ����ǿ������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶������п��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
����ѧ��Ӧԭ����һ���У�����ѧϰ��������Ҫ�Ķ���ʵ�顣��ش��������⣺
I.ij��ѧ��ȤС��Ҫ����к��ȵIJⶨ��
��1��ʵ�����ϱ����ձ�����С�����ձ�������ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β�������0.5mol��L-1 ���ᡢ0.55mol��L-1 NaOH��Һ����ȱ�ٵ�ʵ�鲣����Ʒ�� �� ��
��2��ʵ�����ܷ��û���ͭ˿��������滷�β���������� ����ܡ�������ԭ���� ��
��3�����Ǽ�¼��ʵ���������£�
ʵ �� �Լ����� | �� Һ �� �� | �к��� ��H | ||||
t1 | t2 | |||||
�� | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20�� | 23.3�� | ||
�� | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20�� | 23.5�� | ||
��֪��Q���ţ�=C m(t2 -t1)����Ӧ����Һ�ı�����CΪ4.18KJ����-1��Kg-1��mָ��Һ�������������ʵ��ܶȾ�Ϊ1g��cm-3��
�ټ��������H= ��(�������3λ��Ч����)
�ڸ���ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ��
II.Ϊ�˲ⶨ����H2C2O4��2H2O��KHC2O4��K2SO4�������и����ʵ�������������������ʵ�飺
�ٳ�ȡ6.0 g��������ˮ�ܽ⣬���250 mL������Һ��
������ʽ�ζ�����ȡ25.00 mL������Һ������ƿ�У�������2~3�η�̪��Һ����0.2500 mol/L NaOH��Һ�ζ�������NaOH��Һ20.00 mL��
����ȡ25.00 mL������Һ������һ��ƿ�У���0.1000 mol/L�����Ը��������Һ�ζ������ĸ��������Һ16.00 mL��
�ش��������⣺
��1����֪��0.10 mol/L KHC2O4��ҺpHԼΪ3�����к�̼Ԫ�ص�����Ũ���ɴ�С��˳��Ϊ
��2�� ��ɲ���ƽ�������ӷ���ʽ
C2O42- + MnO4- + H+ = CO2 + Mn2+ +
��3�� ���������ȡ������Һʱ����ʽ�ζ���������ˮϴ����û����ϴ�����õ�H2C2O4��2H2O���������� �����ƫ����ƫС������Ӱ�족��
��4�� ��������жϵζ��յ�ķ����� ��
��5��������0.01 mol/L��H2C2O4��KHC2O4��K2C2O4��Һ��pH���±���ʾ
��д��H2C2O4�ĵ��뷽��ʽ_________ __________________��
��KHC2O4��Һ�����Ե�ԭ���� (���÷���ʽ����ϱ�Ҫ�����ֻش��С��) _______________
����0.1 mol/L�IJ��������Һ��μ�NaOH��Һ�����ԣ���ʱ��Һ�������Ũ�ȹ�ϵ��ȷ����______��
A��c K+) = c(HC2O4-) + c(H2C2O4) + c(C2O42-)
B��c(Na+) = c(H2C2O4) + c(C2O42-)
C��c(K+) + c(Na+) = c(HC2O4-) + c(C2O42-)
D��c(K+) > c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ׯ���и߶�10��ѧ����黯ѧ���������棩 ���ͣ�ѡ����
������������ȷ����
A���Ȼ�ѧ����ʽ�еĻ�ѧ��������ʾ���ʵ����������Ƿ���
B��Ӧ�ø�˹���ɿɼ���ijЩ����ֱ�Ӳ����ķ�Ӧ�ʱ�
C����֪C(ʯī��s)===C(���ʯ��s) ��H��0������ʯ��ʯī�ȶ�
D����֪2H2(g)��O2(g)===2H2O(l) ��H����571.6 kJ/mol����������ȼ����Ϊ285.8 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭���߰���ѧ��һ�����л�ѧ�����ص�ࣩ�������棩 ���ͣ������
���ݷ�Ӧ3Cu��8HNO3(ϡ)=3Cu(NO3)2��2NO����4H2O���ش��������⣺
��1����ԭ����________����ԭ������________����������________������������________��
��2����ԭ���뻹ԭ��������ʵ���֮����________��
��3������8 mol HNO3�μӷ�Ӧʱ�������������ʵ�����Ϊ________g����Ӧ��ת�Ƶĵ��ӵ����ʵ���Ϊ________ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������һ��ѧ��һ�ϵڶ����¿���ѧ���������棩 ���ͣ�ѡ����
������������PbO2��MnSO4��Pb(NO3)2��PbSO4��HNO3��HMnO4��H2O���һ����ѧ����ʽ����֪PbO2����������Ϊ��Ӧ�PbSO4������ˮ�������ж���ȷ���� �� ��
A��Pb(NO3)2�Ƿ�Ӧ�HNO3��������
B��HMnO4�Ƿ�Ӧ�MnSO4��������
C��HNO3�Ƿ�Ӧ�H2O��������
D��H2O�Ƿ�Ӧ�HMnO4��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꺣�Ϲ�����ѧ�߶��ϵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ڹ����·���ȡ����Ӧ���õ�������ȴ����������
A��10�� B��9�� C��8�� D��7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʦ���и�����ѧ�ڵڶ���ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ�����������ȷ����( )
A�����ڿ�����������ȼ�գ�����Գʻ�ɫ�������ɹ�����ɫ��ͬ
B�����Ʊ�����ˮ��Ũ��������»��������������ɷ���������
C��������������ƶ���ʹƷ����Һ��ɫ����ԭ���Dz���ͬ��
D��Mg��CO2��ȼ������MgO��C���ڸ÷�Ӧ�����£�Mg�Ļ�ԭ��ǿ��C�Ļ�ԭ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com